Axit cacbonic | H2CO3 (Là gì, TCHH, Ứng dụng, Mạnh hay yếu, Mindmap)
 8/1/2024
8/1/2024
Tổng hợp kiến thức về cacbonic (H2CO3) : Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học.
Axit cacbonic là gì?
- Khái niệm: Acid carbonic là một hợp chất vô cơ có công thức hóa học H2CO3. Ngoài ra nó còn được gọi là dung dịch carbon
dioxide trong nước, do dung dịch chứa một lượng nhỏ H2CO3.
- Acid carbonic tạo thành hai loại muối là carbonat và bicarbonat.
- Cấu tạo phân tử:
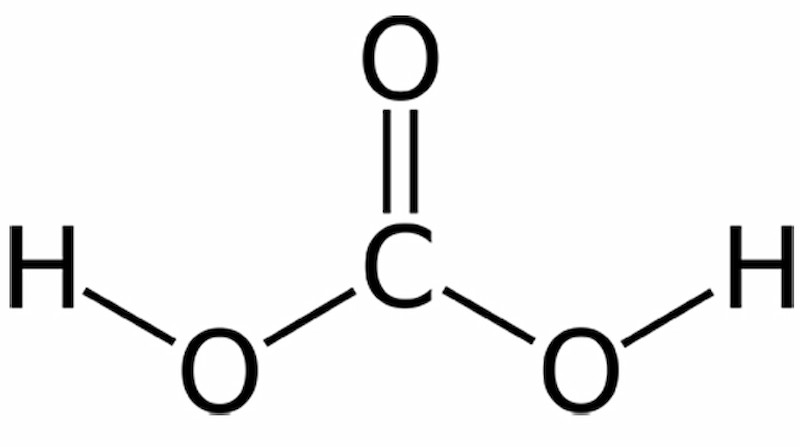
Tính chất vật lý của Axit cacbonic
- Trong tự nhiên axit cacbonic sẽ có trong đá và hang động, trong than đá, thiên thạch, núi lửa, mưa axit, nước ngầm, đại dương,
biển, hồ, sông và thực vật và trong cơ thể con người.
- Khí CO2 có trong máu kết hợp với nước tạo thành axit cacbonic, sau đó được thở ra dưới dạng khí của phổi.
- Khi trời mưa, một lượng H2CO3 sẽ được tạo ra và có lẫn trong không khí:
+ Trong nước mưa và nước tự nhiên khí CO2 được hòa tan: Khoảng 90 cm3 khi CO2 sẽ hòa tan 1000 cm3 nước.
+ Một phần khí CO2 tác dụng với nước tạo thành axit cacbonic, phần lớn khí CO2 còn lại vẫn tồn tại trong khí quyển.
+ Axit cacbonic chỉ tồn tại trong dung dịch nước, nó không thể cô lập các hợp chất tinh khiết.
Tính chất hóa học của Axit cacbonic
- Axit cacbonic làm quỳ tím chuyển thành màu đỏ nhạt vì đây là axit yếu ( tính chất của axit vô cơ)
- H2CO3 là một axit khó tồn tại trong không khí và không bền. Axit cacbonic tạo thành trong các phản ứng hóa học sẽ bị phân
hủy ngay thành CO2 và nước trong điều kiện thường: H2CO3 → CO2 + H2O
Là một axit lưỡng cực, axit cacbonic có thể tạo thành hai loại muối, cacbonat và bicacbonat. Việc bổ sung bazơ vào một lượng dư axit cacbonic sẽ tạo ra muối bicarbonate, trong khi việc bổ sung bazơ dư thừa vào axit cacbonic sẽ tạo ra muối cacbonat
Axit cacbonic là axit mạnh hay yếu?
- Axit cacbonic là một axit yếu nên nó làm cho quỳ tím chuyển thành màu đỏ nhạt.
Cách nhận biết axit cacbonic (H2CO3)
Vì axit cacbonic là một axit yếu nên không phân li hoàn toàn trong nước:
H2CO3 ⇄ H+ +HCO3-
Axit cacbonic cũng không bền, dễ bị phân hủy:
H2CO3 → CO2↑ + H2O ( xúc tác nhiệt độ)
- Chúng ta có thể dùng quỳ tím để nhận biết vì nó sẽ làm quỳ tím hóa đỏ nhạt.
- Dùng dung dịch Ca(OH)2 hoặc Ba(OH)2 dư tác dụng với chất axit cacbonic sẽ xuất hiện kết tủa trắng.
Phương pháp điều chế
- Vì axit cacbonic là một axit rất yếu nên nó không tồn tại được lâu.
- Cho CO2 phản ứng với nước để thu được axit cacbonic theo phương trình sau:
H2O + CO2 → H2CO3
Ứng dụng
- H2CO3 có thể hòa tan đá vôi nên nó sẽ tạo nên nhiều hình thù của đá vôi như măng đá và nhũ đá.
- Được sử dụng trong nhiều loại nước uống có gas như 7up, coca,...
- Ngoài ra còn xuất hiện trong thành phần của thực phẩm lên men dưới dạng chất thải được tạo ra bởi vi khuẩn ăn thức ăn.
- Đóng góp vai trò trong tính axit cao của soda.
- Tròn đời sống thường ngày H2CO3 được sử dụng trong nhiều lĩnh vực khác như mỹ phẩm, dược phẩm, chế biến thực phẩm, phân
bón, thuốc gây mê,..
Sử dụng Axit cacbonic đúng cách
- Axit cacbonic là chất không độc hại hoặc nguy hiểm đến con người. Nhưng khi tiếp xúc với nồng độ cao có thể gây kích ứng mắt
và đường hô hấp. Vì vậy chúng ta phải chuẩn bị đồ bảo hộ khi tiếp xúc axit ở nồng độ cao.
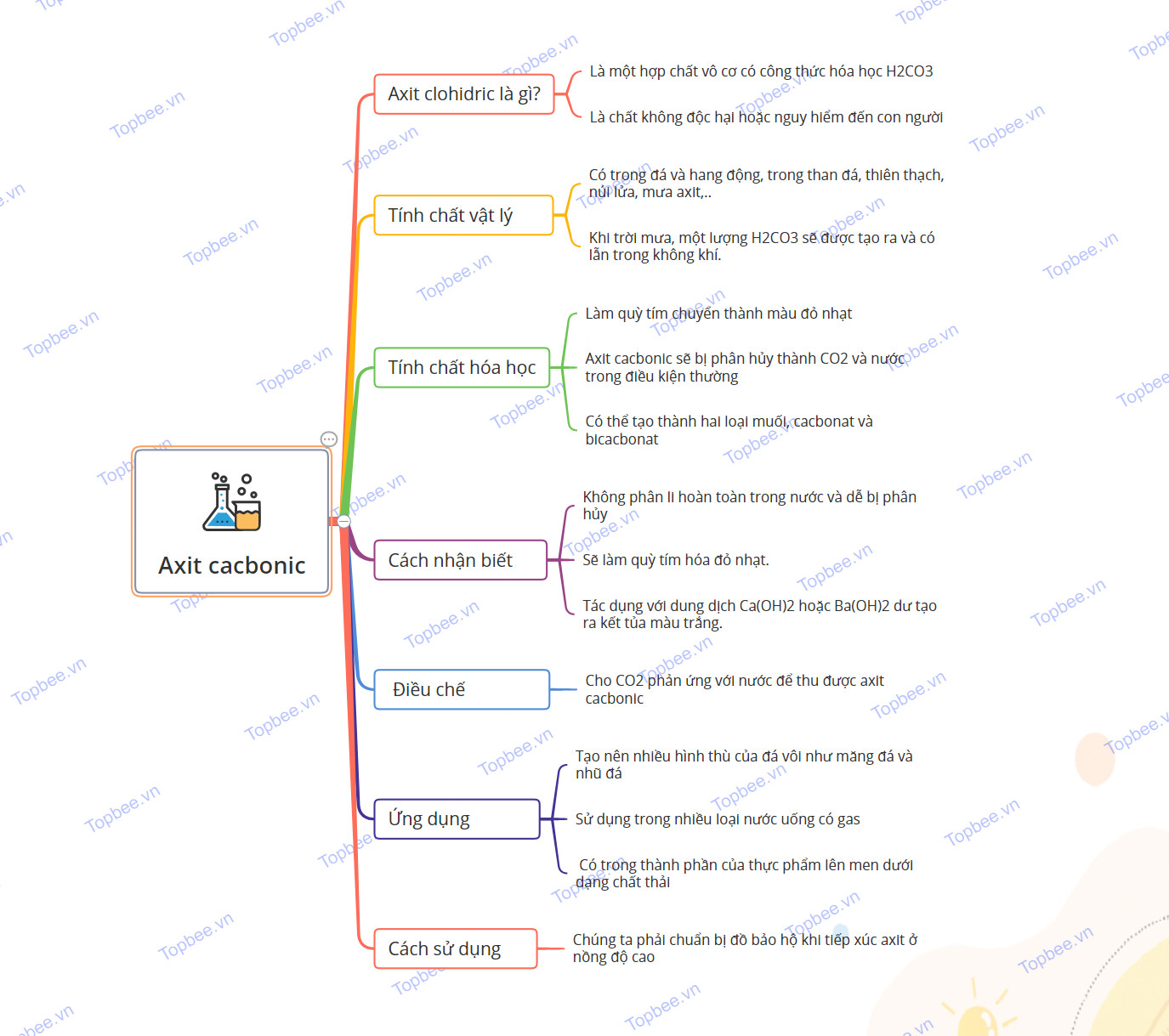
Sơ đồ tư duy về axit cacbonic