Axit hydrobromic | HBr (Là gì, TCHH, Ứng dụng, Mạnh hay yếu, Mindmap)
 9/1/2024
9/1/2024
Tổng hợp kiến thức về Axit hydrobromic (HBr) : Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học.
Axit hydrobromic là gì?
- Khái niệm: Axit hydrobromic là một axit vô cơ rất mạnh vì liên kết cộng hóa trị có thể dễ dàng bị ion hóa do độ âm điện lớn của
nguyên tử Brom. Nó có tính ăn mòn cao và được hình thành trong nước bằng cách hòa tan bromide hydro.
- Công thức hóa học của Axit Hydrobromic là HBr.
- Cấu tạo phân tử:

Tính chất vật lý của Axit hydrobromic
- Axit hydrobromic có mùi khó chịu hăng và tồn tại dưới dạng chất lỏng màu vàng không màu.
- Thể hiện tính mạnh hơn axit iothidric nhưng lại yếu hơn axit clohydric : HI>HBr>HCl.
- Khối lượng riêng là 1,49 g/cm3.
- Trọng lượng phân tử: 80,91 g/mol.
- Nhiệt độ sôi: 122 độ C ở 700mmHg.
- Nhiệt độ nóng chảy: -11 độ C.
- Độ axit pKa: -9 thể hiện tính axit mạnh.
- Là chất có tính ăn mòn cao, không bắt lửa và an tốt trong nước.
Tính chất hóa học của Axit hydrobromic
- Axit hydrobromic làm đổi màu chất chỉ thị màu và quỳ tím chuyển sang màu đỏ.
- Tác dụng với kim loại tạo ra sản phẩm là muối bromide và giải phóng khí H2. ( Chỉ tác dụng được với những kim loại đứng trước
nguyên tử H trong dãy hoạt động hoá học kim loại)
2HBr + 2Na → 2NaBr + H2
- Tác dụng với oxit bazơ sinh ra muối bromide và nước:
Na2O + 2HBr → 2NaBr + H2O
- Tác dụng với bazơ tạo ra sản phẩm là muối và nước:
Mg(OH)2 + 2HBr → MgBr2+ 2H2O
- Tác dụng với muối sinh ra muối mới và axit:
K2CO3 + 2HBr → 2KBr + H2O + CO2
AgNO3 + HBr → AgBr (kết tủa) + HNO3
Để phản ứng trên xảy ra cần thoả mãn điều kiện sau:
+ Muối phải tan được trong nước thì được tham gia vào quá trình phản ứng.
+ Sản phẩm tạo ra phải là muối kết tủa hoặc axit yếu.
- Tác dụng với nguyên tố phi kim:
Cl2 + 2HBr → Br2 + 2HCl
Axit hydrobromic là axit mạnh hay yếu?
- Axit hydrobromic là một axit vô cơ rất mạnh được hình thành trong nước bằng cách hòa tan bromide hydro
Cách nhận biết Axit hydrobromic (HBr)
- Dung dịch axit hydrobromic làm quỳ tím chuyển sang màu đỏ.
- Cho dung dịch axit hydrobromic tác dụng với Bạc nitrat sẽ tạo ra muối kết tủa màu trắng.
Phương pháp điều chế
- Quá trình phản ứng của khí brom, SO2 và nước sẽ tạo ra sản phẩm là HBr như phương trình sau:
Br2 + SO2 + 2H2O → H2SO4 + 2HBr
- Hoà tan khí hiđrô bromide trong nước cũng sẽ tạo ra axit hydrobromic .
- Cho Br2 phản ứng với lưu huỳnh hoặc photpho trong nước sinh ra HBr.
PBr3 + 3H2O → H3PO3 + 3HBr
Ứng dụng
- Dùng để điều chế muối bromua, đặc biệt là kẽm bromua, canxi bromua và natri bromua
- Điều chế các hợp chất brom hữu cơ.
- Là nguyên liệu chính để sản xuất muối bromua, nhất là kẽm bromua, canxi bromua cũng như natri bromua…
- Đây là chất để tổng hợp các hợp chất brom hữu cơ nên được sử dụng nhiều trong viện nghiên cứu, phòng thí nghiệm, tham gia
trong nhiều phản ứng.
- Ngoài ra đây là chất xúc tác cho phản ứng alkyl hóa giúp cho quá trình khai thác quặng.
Sử dụng Axit hydrobromic đúng cách
- Quy tắc sử dụng Axit clohidric đúng cách
+ Bật quạt thông gió trong tủ an toàn sinh học trước khi tiến hành lấy axit để thí nghiệm.
+ Chuẩn bị đầy đủ các đồ bảo hộ để tránh axit bắn vào người.
+ Trong trường hợp dính phải axit hãy rửa ngay với nước sạch rồi đến ngay gần cơ sở y tế gần nhất để có hướng xử lý thích hợp.
+ Không đổ axit bừa bãi vào bồn rửa vì có thể làm hỏng đường ống, hãy đổ đúng nơi quy định. ( Do có tính chất ăn mòn)
- Cách bảo quản Axit clohidric: Bảo quản nơi khô ráo, thoáng mát nhiệt độ từ 15-25 độ C là phù hợp.
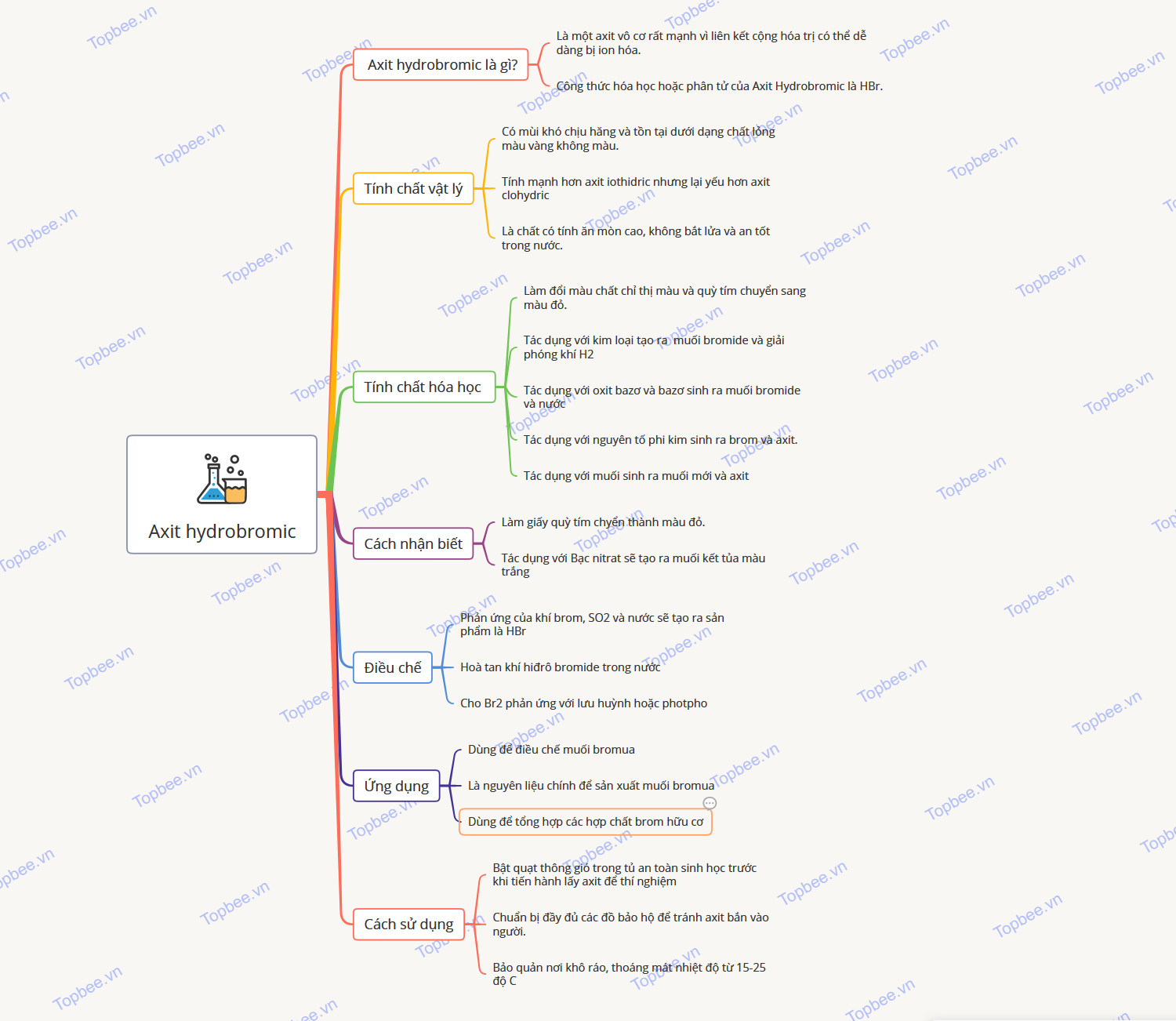
Sơ đồ tư duy về axit hydrobromic