

K2SO3 + BaCl2 → 2KCl + BaSO3( ↓) | Cân bằng PTHH Potassium sulfite
 27/6/2024
27/6/2024
Cân bằng PTHH: K2SO3 + BaCl2 → 2KCl + BaSO3( ↓) chính xác và dễ hiểu nhất kèm theo bài tập vận dụng có đáp án chi tiết
1. Loại phản ứng
Phản ứng trao đổi
2. Cân bằng PTHH:
K2SO3 + BaCl2 → 2KCl + BaSO3( ↓)
3. Điều kiện xảy ra phản ứng/ Xúc tác phản ứng
Điều kiện thường.
4. Cách tiến hành thí nghiệm
Nhỏ dung dịch K2SO3 vào ống nghiệm chứa BaCl2
5. Chất tạo ra từ phản ứng:
- KCl là một chất rắn tinh thể màu trắng ở nhiệt độ phòng, tan trong nước và các dung môi phân cực khác.
- BaSO3 là một chất rắn vô cơ có màu trắng, tinh thể, không tan trong nước và chịu được nhiệt độ cao.
6. Hiện tượng quan sát từ phản ứng
Có kết tủa trắng.
7. Ứng dụng của PTHH trên
- Phương trình hóa học trên được ứng dụng là chất độn trong cao su, nhựa và dùng trong sản xuất giấy, thủy tinh và gốm sứ,... Ngoài ra còn sử dụng trong sản xuất phân bón, hóa chất và dược phẩm.
8. Bài tập vận dụng
Bài tập 1: Nhỏ từ từ một vài giọt K2SO3 vào ống nghiệm có chứa 1ml BaCl2 thu được kết tủa có màu
A. trắng.B. đen.C. vàng.D. nâu đỏ.
Lời giải
K2SO3 + BaCl2 → 2KCl + BaSO3( ↓)
BaSO3( ↓) trắng
Đáp án A.
Bài tập 2: Chất nào sau đây không thể phản ứng với K2SO3?
BaCl2.B. Ba(OH)2.C. Ba(NO3)2.D, BaSO3
Lời giải
BaSO3 không phản ứng với K2SO3.
Đáp án D.
Bài tập 3: Khối lượng kết tủa thu được khi cho K2SO3 phản ứng vừa đủ với 100ml BaCl2 0,01M là
A. 2,33g.B. 2,17g.C.1,33g.D. 0,217g
Lời giải
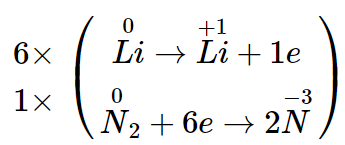
Đáp án D.





