

Khí Etan | C2H6 (Là gì, TCVL, hóa học, điều chế, ứng dụng, mindmap)
 10/1/2024
10/1/2024
Tổng hợp kiến thức về khí etan (C2H6): Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học.
Etan là gì?
- Khái niệm: Etan là một hợp chất hydrocacbon no không tạo vòng và nằm trong dãy đồng đẳng của ankan. Có công thức hóa học kí hiệu là C2H6.
- Cấu tạo phân tử:
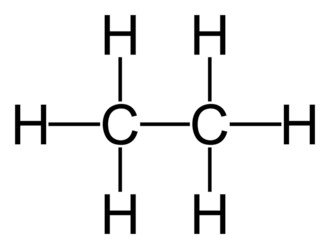
- Danh pháp:
+ Tên quốc tế gọi là etan: C2H6.
+ Tên gốc Ankyl được gọi là etyl: CH3CH2.
Trạng thái tự nhiên
- Theo các nhà nghiên cứu đã chỉ ra rằng etan chiếm 10% thành phần của khí thiên nhiên
- Ngoài ra etan được sản xuất từ chưng cất dầu mỏ. Trong phòng thí nghiệm nó có thể được tổng hợp hóa học bằng điện phân Kolbe.
Tính chất vật lý
- Etan thường tồn tại dưới dạng khí không màu không mùi ở nhiệt độ và áp suất lý tưởng. Ngoài ra nó còn bị chuyển từ dạng khí sang dạng lỏng hoặc rắn khi được làm lạnh và nén.
- Etan nhẹ hơn nước, hầu như không thể tan trong nước vì vậy mà người ta hay gọi là kị nước.
Tính chất hóa học
Phản ứng thế bởi halogen
- Khi chiếu sáng hoặc đốt nóng hỗn hợp etan và brom sẽ xảy ra phản ứng thế lần lượt các nguyên tử hidro bằng brom, cụ thể như phương trình sau:
C2H6 + Br2 → C2H5Br + HBr
Phản ứng tách (gãy liên kết C-C và C-H)
CH3 - CH3 → CH2=CH2 + H2 ( Điều kiện có chất xúc tác và 500oC )
Phản ứng oxi hóa
- Khi đốt etan bị cháy sinh ra CO2, H2O và tỏa nhiệt.
C2H6 + 7/2 O2 → 2 CO2 + 3H2O (Điều kiện phản ứng có nhiệt)
- Trong quá trình nếu không đủ oxi, ankan bị cháy không hoàn toàn, khi đó ngoài CO2 và H2O còn tạo ra các sản phẩm như CO, than muội, không những làm giảm năng suất tỏa nhiệt mà còn gây độc hại cho môi trường.
Cách nhận biết
- Đốt cháy khí etan rồi cho sản phẩm vào dung dịch Ca(OH)2 rồi sẽ xuất hiện kết tủa vẩn đục trắng, khi đó ta sẽ nhận biết được khí metan.
C2H6 + 7/2 O2 → 2 CO2 + 3H2O
CO2 + Ca(OH)2 → CaCO3 + H
- Cho khí etan tác dụng với clo dưới ánh sáng. Lấy sản phẩm vừa tạo ra cho vào quỳ tím ẩm, nếu quỳ hóa đỏ thì ta sẽ nhận biết được khí etan.
C2H6 + Cl2 → C2H5Cl + HCl
Điều chế
- Etan và các đồng đẳng được tách từ khí thiên nhiên và dầu mỏ.
- Etan cũng được tạo ra từ các phản ứng trong phòng thí nghiệm:
2CH3Cl + 2Na → C2H6 + 2NaCl
C2H4 + H2 → C2H6 ( Điều kiện phản ứng có chất xúc tác và nhiệt độ)
C4H10 → C2H6 + C2H4 ( Điều kiện phản ứng có chất xúc tác và 500oC)
C2H2 + 2H2 → C2H6 ( Điều kiện phản ứng có chất xúc tác và nhiệt độ)
C2H5COONa + NaOH → C2H6 + NaCO3
Ứng dụng
- Chế biến dầu thô bắt đầu từ khí thiên nhiên sau đó nó được chế biến thành các sản phẩm khác nhau, ví dụ như xăng.
- Làm nhiên liệu trong các động cơ đốt trong và là dung môi tốt cho các chất không phân cực.
- Ngoài ra có thể chuyển hóa thành etylen nhờ phản ứng cracking.
Sơ đồ tư duy của khí etan
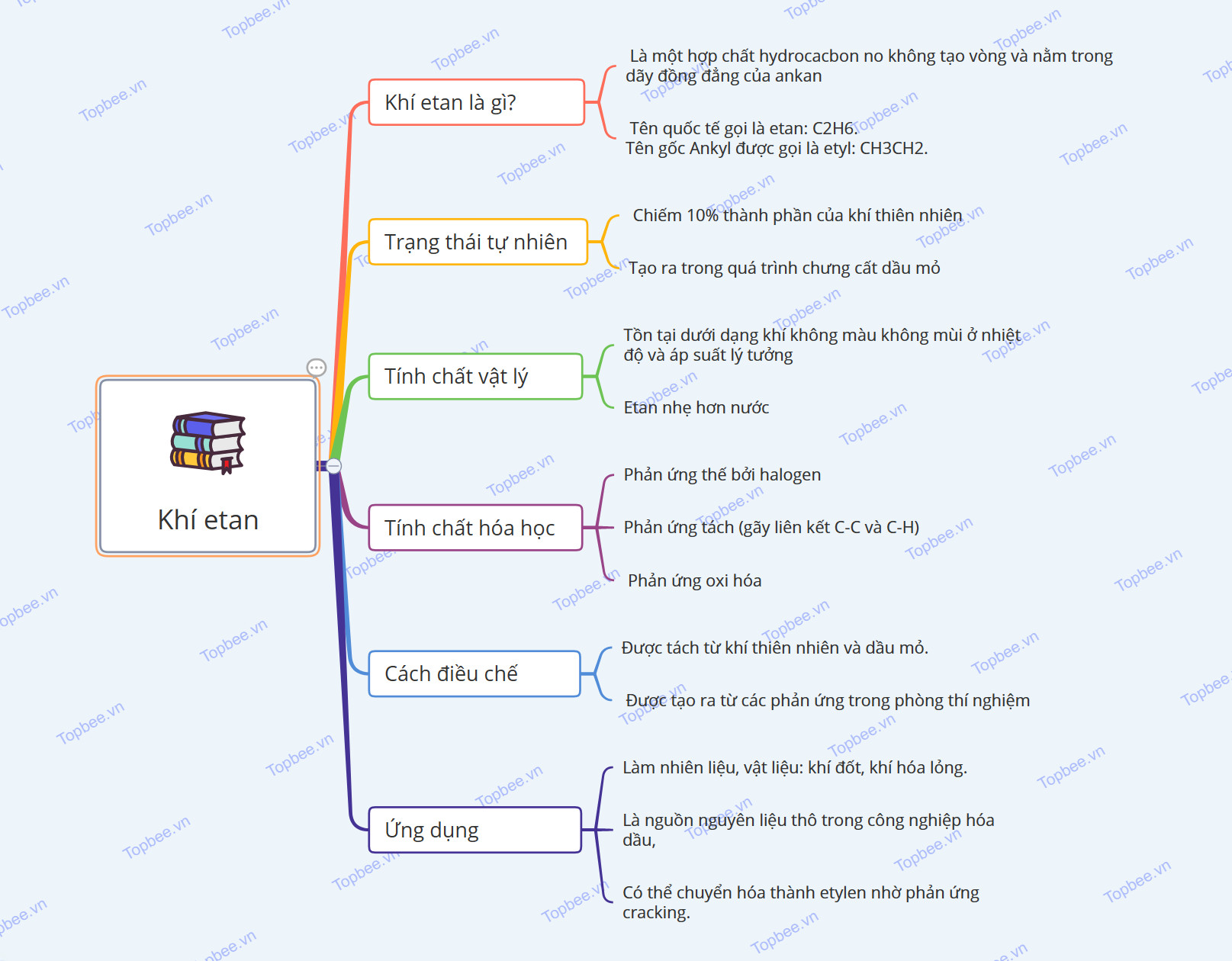
Một số câu hỏi liên quan đên khí etan
Câu 1: Nhận xét nào đúng khi nói về tính tan của etan trong nước?
A. Không tan
B. Tan ít
C. Tan nhiều
D. Không tan
Câu 2: Tính thể tích khí oxy cần dùng và thể tích của khí cacbonic được tạo ra khi đốt cháy hoàn toàn 11,2 lít khí
C2H6 (đktc). Biết rằng thể tích các khí đều được đo ở đktc
Câu 3: Cho một hỗn hợp khí gồm khí CO2 và C2H6. Hãy trình bày phương pháp hóa học để có thể:
a) Thu được khí C2H6
b) Thu được khí CO2





