NH3 (kết tủa không, điện ly mạnh hay yếu, mindmap)
 11/1/2024
11/1/2024
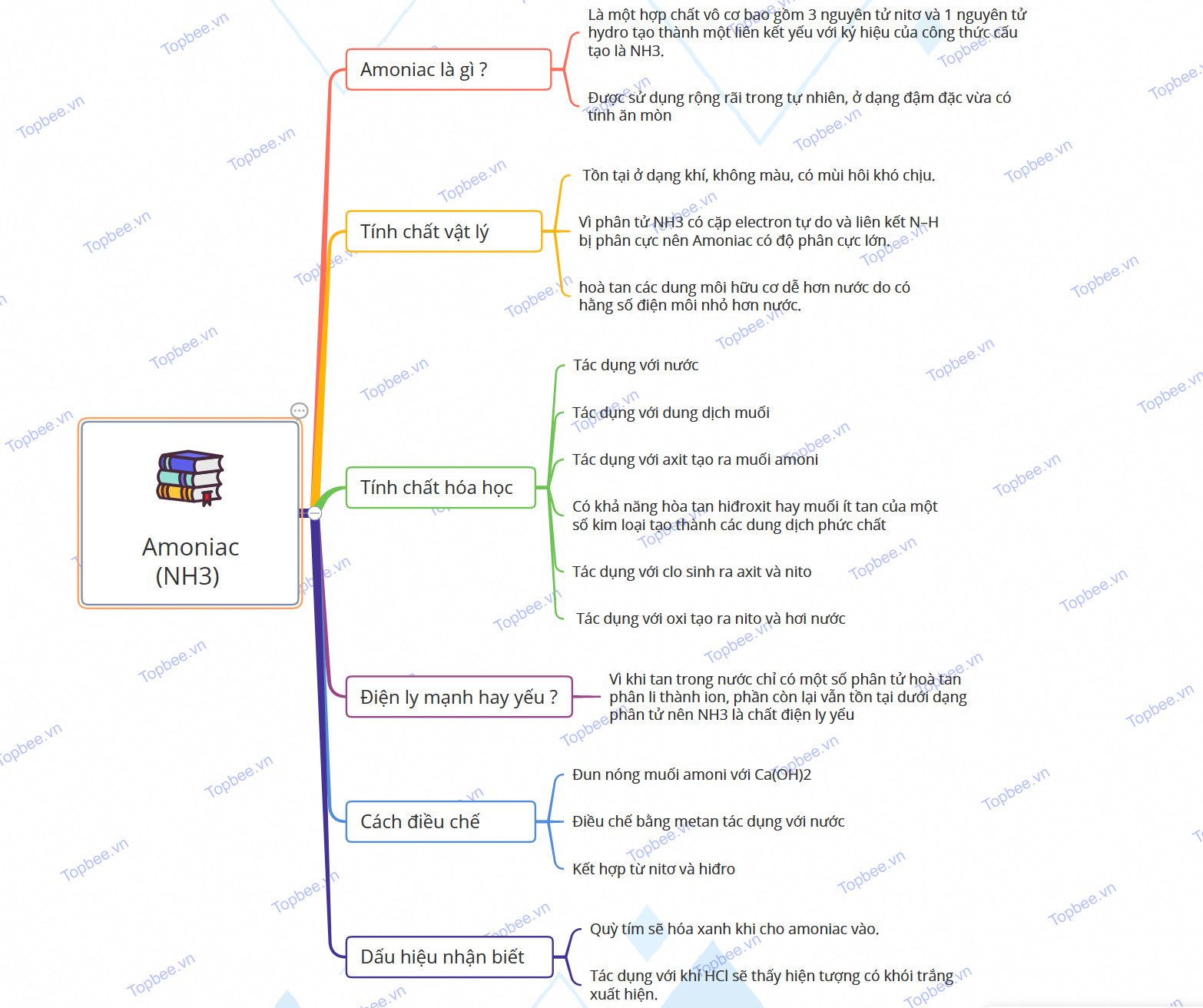
Tổng hợp kiến thức về NH3: Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức
Amoniac (NH3) là gì ?
- Khái niệm: Amoniac là một hợp chất vô cơ bao gồm 3 nguyên tử nitơ và 1 nguyên tử hydro tạo thành một liên kết yếu với ký hiệu của công thức cấu tạo là NH3.
- Cấu tạo phân tử:
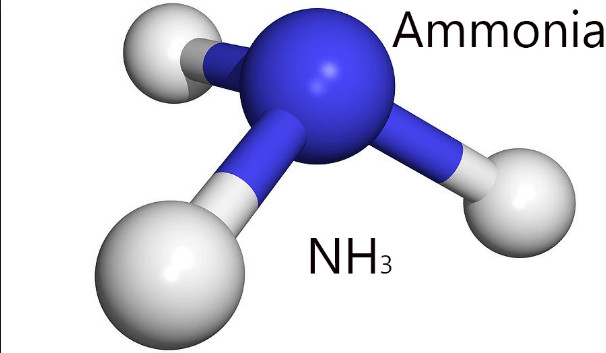
- Được sử dụng rộng rãi trong tự nhiên, ở dạng đậm đặc vừa có tính ăn mòn
Tính chất vật lý
- Amoniac thường tồn tại ở dạng khí, không màu, có mùi hôi khó chịu.
- Với mức nồng độ lớn amoniac có thể gây chết người.
- Vì phân tử NH3 có cặp electron tự do và liên kết N–H bị phân cực nên Amoniac có độ phân cực lớn. Vì vậy NH3 là chất dễ hoá lỏng.
- Amoniac hoà tan các dung môi hữu cơ dễ hơn nước do có hằng số điện môi nhỏ hơn nước.
Tính chất hóa học
- Tác dụng với nước:
NH3 + H2O ⇋ NH4+ + OH-
- Dung dịch NH3 là một dung dịch bazơ yếu.
- Tác dụng với dung dịch muối (muối của những kim loại có hidroxit không tan):
AlCl3 + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4Cl
Al3+ + 3NH3 + 3H2O → Al(OH)3↓ + 3NH4+
- Tác dụng với axit tạo ra muối amoni:
NH3 + HCl → NH4Cl (amoni clorua)
2NH3 + H2SO4 → (NH4)2SO4 (amoni sunfat)
- Có khả năng hòa tan hiđroxit hay muối ít tan của một số kim loại tạo thành các dung dịch phức chất:
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh thẫm)
AgCl + 2NH3 → [Ag(NH3)2]Cl
- Tác dụng với oxi tạo ra nito và hơi nước:
NH3 + 3O2 → 2N2 + 6H2O ( đkpu là nhiệt độ)
4NH3 + 5O2 → 4NO + 6H2O ( có chất xúc tác và nhiệt độ)
- Tác dụng với clo sinh ra axit và nito:
2NH3 + 3Cl2 → N2 + 6HCl
- Tác dụng với CuO:
2NH3 + 2CuO → 2Cu + N2 + 3H2O (đkpu là nhiệt độ)
Amoniac (NH3) là chất điện ly mạnh hay yếu ?
- Vì khi tan trong nước chỉ có một số phân tử hoà tan phân li thành ion, phần còn lại vẫn tồn tại dưới dạng phân tử nên NH3 là chất điện ly yếu:
NH3 + H2O ⇆ NH4+ + OH−
Amoniac (NH3) có kết tủa không ?
- Amoniac không là chất kết tủa và khi dùng dư NH3 ta không thu được kết tủa sau phản ứng.
PTHH thường gặp
NH3 + Cl2 → N2 + NH4Cl
NH3 + O2 → NO + H2O
NH3 + HCl → NH4Cl
NH3 + H2O → NH4OH
NH3 + AlCl3 + H2O → Al(OH)3 + NH4Cl
Phương pháp điều chế
- Đun nóng muối amoni với Ca(OH)2:
2NH4Cl + Ca(OH)2 → NH3 + CaCl2 + H2
- Điều chế bằng metan tác dụng với nước
CH4 + H2O → CO + 3H2 (xúc tác Ni, nhiệt độ cao)
- Kết hợp từ nitơ và hiđro :
N2 + 3H2 → 2NH3 (ΔH = –92 kJ/mol)
Dấu hiệu nhận biết
- Quỳ tím sẽ hóa xanh khi cho amoniac vào.
- Ngoài ra nhận biết khí NH3 bằng cách cho tác dụng với khí HCl sẽ thấy hiện tượng có khói trắng xuất hiện.
Sơ đồ tư duy của Amoniac (NH3)