

2KOH + SO2 → K2SO3 + H2O | Cân bằng PTHH Potassium hydroxide
 24/6/2024
24/6/2024
Cân bằng PTHH: 2KOH + SO2 → K2SO3 + H2O chính xác và dễ hiểu nhất kèm theo bài tập vận dụng có đáp án chi tiết
1. Loại phản ứng
Phản ứng trao đổi.
2. Cân bằng PTHH:
2KOH + SO2 → K2SO3 + H2O
3. Điều kiện xảy ra phản ứng/ Xúc tác phản ứng
Phản ứng xảy ra ngay điều kiện thường.
4. Cách tiến hành thí nghiệm
Dẫn khí SO2 vào ống nghiệm chứa KOH và vài giọt chất chỉ thị.
5. Chất tạo ra từ phản ứng:
K2SO3 là một hợp chất muối vô cơ tồn tại ở trạng thái rắn, màu trắng, tan tốt trong nước và có tính khử nhẹ.
6. Hiện tượng quan sát từ phản ứng
Quan sát sự chuyển màu của chỉ thị phù hợp trước và sau phản ứng.
7. Ứng dụng của PTHH trên
K2SO3 làm chất bảo quản thực phẩm, chất tẩy trắng trong công nghiệp dệt may và xử lý nước,...
8. Bài tập vận dụng
Bài tập 1: Cho 2,24 lít khí SO2 ở đktc phản ứng với lượng dư dung dịch KOH thu được dung dịch X. Khối lượng muối tan có trong X là
A.15,8 gam.B. 13,8 gam.C. 11,8 gam.D. 10,8 gam.
Lời giải
Do KOH dư nên có phản ứng
mmuối = 0,1.158 = 15,8 gam.
Đáp án A.
Bài tập 2: Cho SO2 tác dụng với lượng dư dung dịch KOH thu được dung dịch X. Chất tan có trong dung dịch X là
A.K2SO3.B. K2SO3 và KHSO3.C. KHSO3.D. K2SO3 và KOH.
Lời giải
Do KOH dư nên có phản ứng
2KOH + SO2 → K2SO3 + H2O
Chất tan có trong dung dịch X là K2SO3 và KOH dư.
Đáp án D.
Bài tập 3: Cho 2,24 lít khí SO2 ở đktc phản ứng với dung dịch chứa 0,3 mol KOH. Khối lượng muối tan có trong dung dịch sau phản ứng là
A.15,8 gam.B. 13,8 gam.C. 11,8 gam.D. 10,8 gam.
Lời giải
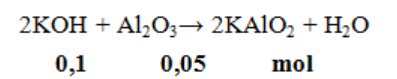
mmuối = 0,1.158 = 15,8 gam.
Đáp án A.





