

2KOH + Zn(OH)2 → K2ZnO2+ 2H2O | Cân bằng PTHH Potassium hydroxide
 24/6/2024
24/6/2024
Cân bằng PTHH: 2KOH + Zn(OH)2 → K2ZnO2+ 2H2O chính xác và dễ hiểu nhất kèm theo bài tập vận dụng có đáp án chi tiết
1. Loại phản ứng
Phản ứng trao đổi.
2. Cân bằng PTHH:
2KOH + Zn(OH)2 → K2ZnO2+ 2H2O
3. Điều kiện xảy ra phản ứng/ Xúc tác phản ứng
Phản ứng xảy ra ngay điều kiện thường.
4. Cách tiến hành thí nghiệm
Nhỏ từ từ dung dịch KOH vào ống nghiệm chứa Zn(OH)2
5. Chất tạo ra từ phản ứng:
K2ZnO2 là chất rắn màu trắng, không tan trong nước nhưng tan trong axit.
6. Hiện tượng quan sát từ phản ứng
Kết tủa tan dần tạo dung dịch.
7. Ứng dụng của PTHH trên
Phản ứng này có vai trò quan trọng trong xử lý nước thải, loại bỏ các ion kim loại nặng chẳng hạn như ion kẽm.
8. Bài tập vận dụng
Bài tập 1: Nhỏ từ từ dung dịch KOH đến dư vào ống nghiệm chứa Zn(NO3)2. Hiện tượng thu được sau phản ứng là
A.xuất hiện kết tủa trắng.
B.xuất hiện kết tủa màu nâu đỏ.
C.xuất hiện kết tủa trắng, sau đó kết tủa tan.
D.xuất hiện kết tủa xanh.
Lời giải
2KOH + Zn(NO3)2 → 2KNO3+ Zn(OH)2
Zn(OH)2: kết tủa trắng, sau đó KOH dư, kết tủa tan theo phương trình:
2KOH + Zn(OH)2 → K2ZnO2+ 2H2O
Đáp án C.
Bài tập 2: Phản ứng nào sau đây là phản ứng trao đổi?
A.KOH + Cr(OH)3 → KCrO2+ 2H2O
B.2KOH + Zn(OH)2 → K2ZnO2+ 2H2O
C.2KOH + CuSO4 → K2SO4 + Cu(OH)2
D.KOH + Al(OH)3 → KAlO2+ 2H2O
Lời giải
2KOH + CuSO4 → K2SO4 + Cu(OH)2 là phản ứng trao đổi.
Đáp án C.
Bài tập 3: Số mol KOH cần dung để phản ứng hoàn toàn với 0,99g Zn(OH)2 là
A.0,001.B. 0,01.C. 0,1.D. 1.
Lời giải
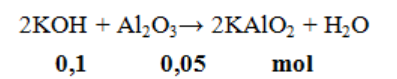
Đáp án B.





