AgNO3 (kết tủa không, điện ly mạnh hay yếu, mindmap)
 11/1/2024
11/1/2024
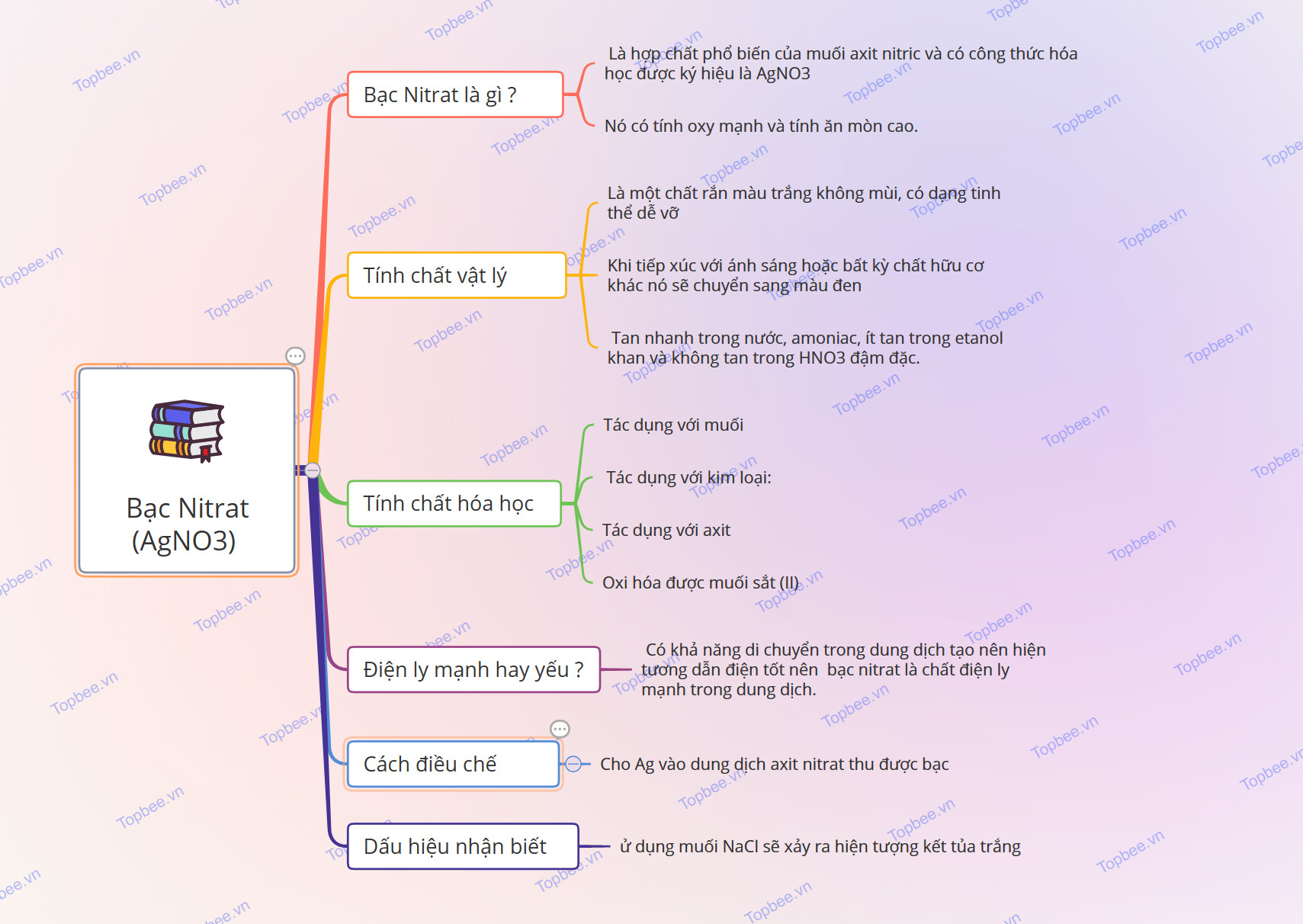
Tổng hợp kiến thức về AgNO3: Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức
Bạc Nitrat (AgNO3) là gì ?
- Khái niệm: Bạc Nitrat là hợp chất phổ biến của muối axit nitric và có công thức hóa học được ký hiệu là AgNO3. Nó có tính oxy mạnh và tính ăn mòn cao.
Cấu tạo phân tử:
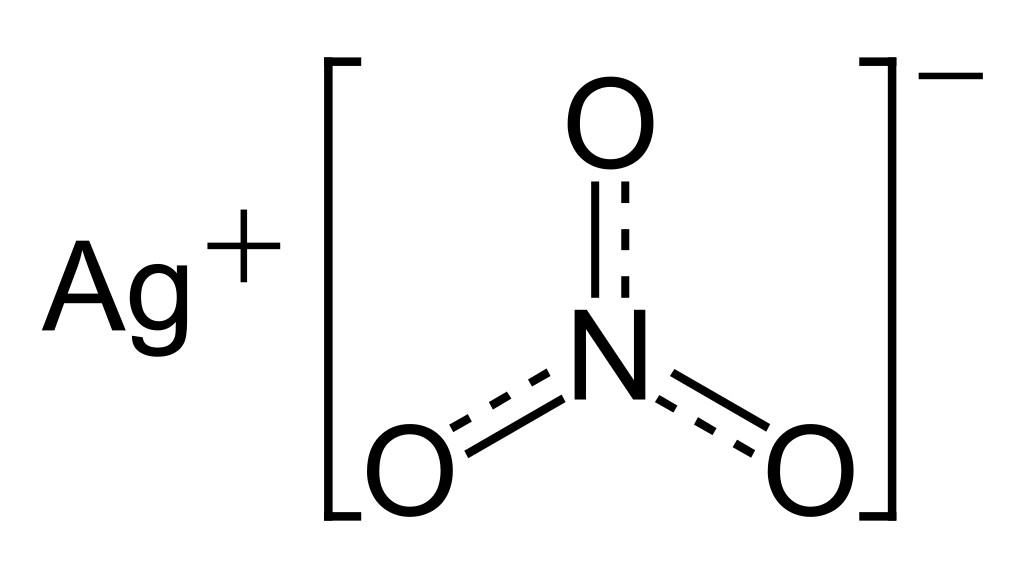
Tính chất vật lý
- Bạc nitrat là một chất rắn màu trắng không mùi, có dạng tinh thể dễ vỡ hình kim hoặc hình thoi.
- Khi tiếp xúc với ánh sáng hoặc bất kỳ chất hữu cơ khác nó sẽ chuyển sang màu đen.
- AgNO3 sẽ bị phân hủy khi đun nóng.
- Ngoài ra nó còn tan nhanh trong nước, amoniac, ít tan trong etanol khan và không tan trong HNO3 đậm đặc.
- AgNO3 có tính oxy hóa mạnh và tính ăn mòn nhưng tính axit yếu.
- Khối lượng riêng: 5.35 g/cm3
- Khối lượng mol 169,8722 g/mol
- Nhiệt độ sôi: 444 °C (717 K; 831 °F)
- Nhiệt độ nóng chảy: 212 °C (485 K; 414 °F)
Tính chất hóa học
- Tác dụng với muối:
AgNO3 + KCl →AgCl↓ + KNO3
2AgNO3 + CaCl2 →2AgCl↓ + Ca(NO3)2
- Tác dụng với kim loại:
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
- Tác dụng với axit:
AgNO3 + HCl → AgCl ↓ + HNO3
- Oxi hóa được muối sắt (II):
Fe(NO3)2 + AgNO3 → Fe(NO3)3 + Ag
Điện ly mạnh hay yếu ?
Khi tan trong nước, các phân tử AgNO3 sẽ phân li thành ion Ag+ và ion NO3- vì các ion này có khả năng di chuyển trong dung dịch tạo nên hiện tương dẫn điện tốt. Như vậy bạc nitrat là chất điện ly mạnh trong dung dịch.
AgNO3 có kết tủa không?
- Ion bạc (Ag+) trong AgNO3 tác dụng với ion của các chất khác (NaCl, KCl, HCl, hay Cl-) để tạo ra các muối kết tủa như AgCl hoặc AgBr. Như vậy AgNO3 có thể tạo kết tủa khi tác dụng với một số chất khác.
- Cho dung dịch bạc nitrat tác dụng với NaCl sẽ tạo ra muối bạc kết tủa, như phương trình sau:
AgNO3 + NaCl → AgCl + NaNO3
PTHH thường gặp
NaF + AgNO3 → không tác dụng
NaCl + AgNO3 → AgCl (↓ trắng) + NaNO3
AgNO3 + NaN3 ⟶ NaNO3 + AgN3
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
HBr + AgNO3 → AgBr (↓ vàng) + HNO3
HI + AgNO3 → AgI (↓ vàng đậm) + HNO3
Cách điều chế
- Có thể điều chế nitrat trong phòng thí nghiệm, tùy vào mức độ của axit và trong điều kiện có tủ hút khí độc do chất độc nitơ ôxit sinh ra trong phản ứng thực hiện, cụ thể phương trình hóa học như sau:
3 Ag + 4 HNO3(lạnh và loãng) → 3 AgNO3 + 2 H2O + NO
3 Ag + 6 HNO3(đậm đặc, nóng) → 3 AgNO3 + 3 H2O + 3 NO2
Dấu hiệu nhận biết
Để nhận biết muối bạc nitrat thì hãy sử dụng muối NaCl sẽ xảy ra hiện tượng kết tủa trắng:
AgNO3 + NaCl →AgCl↓+ NaNO3
Sơ đồ tư duy của AgNO3