

Flo | F (CTCT, Tính chất vật lí, hóa học, Điều chế, Mindmap)
 26/12/2023
26/12/2023
Bài viết tìm hiểu về Flo (F) do Topbee biên soạn tổng hợp kiến thức trọng tâm về Flo (F): Công thức hóa học, Tính chất vật lí, hóa học, Điều chế, Mindmap giúp học sinh ôn tập và bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học.
Flo tồn tại ở đâu?
+ Flo là nguyên tố hóa học có kí hiệu là F và có số hiệu nguyên tử là 9 trong bảng tuần hoàn hóa học.
+ Flo có trong hợp chất tạo nên men răng của người và các động vật
+ Flo chiếm 0,08% khối lượng vỏ Trái Đất
+ F tồn tại trong các chất khoáng dạng muối florua : CaF2 và AlF3 . 3NaF (criolit).
Cấu tạo nguyên tử
+ Cấu hình electron của Flo (F) là: 1s22s22p5.
+ Nguyên tố F nằm ở ô số 9, nhóm VA, chu kì 2
+ Flo là một phi kim.
+ Cấu hình e của F: lớp ngoài cùng có 7 electron, cần thêm 1 electron để đạt được cấu hình điện tử bền với 8 electron ngoài cùng.
+ F thường có hóa trị -1
Tính chất vật lý
- Flo là chất khí, màu lục nhạt, khí flo rất độc.
- Nguyên tử khối: 19 g/mol
- Flo là phi kim mạnh nhất, độ âm điện lớn nhất, tính oxi hóa mạnh nhất.
- Khí flo nặng hơn không khí, có tính ăn mòn cao.
- Nhiệt độ nóng chảy của Flo: -219,62 0C
- Nhiệt độ sôi: -188,12 0C
- Khối lượng riêng: 1,7 g/cm3.
Tính chất hóa học
*Tác dụng với kim loại và phi kim
+ Flo tác dụng tất cả kim loại kể cả Au và Pt
+ Phản ứng được hầu hết phi kim (trừ O2, N2 và các nguyên tố khí trơ)
Ca + F2 → CaF2
3F2 + S → SF6
3F2 + 2Au → AuF3 (Vàng florua)
F2 + Cu → CuF2 (Đồng (II) florua)
*Tác dụng với hidro:
+ Flo phản ứng hóa học mạnh với hidro hơn các halogen khác tạo ra axit flohydric.
Phản ứng nổ rất mạnh, có thể ngay cả trong bóng tối, nhiệt độ thấp, gây chết người.
H2 + F2 → 2HF
+ Khí HF kết hợp với nước sẽ tạo ra dung dịch HF – đây là loại axit yếu. Dung dịch HF được ứng dụng trong kĩ thuật khắc thủy tinh. Vì khi
nó tác dụng với SiO2 sẽ tạo dung dịch có khả năng ăn mòn thủy tinh.
SiO2 + 4HF → SiF4 (Silic tetrafloru) + 2H2O
*Tác dụng với nước
+ Khí flo qua nước sẽ làm bốc cháy nước (do giải phóng O2).
2F2 + 2H2O → 4HF + O2
Đó cũng là nguyên nhân vì sao F2 không đẩy Cl2, Br2, I2 ra khỏi dung dịch muối hoặc axit mặc dù flo có tính oxi hóa mạnh hơn.
Điều chế
- Flo được khai thác và chế biến từ khoáng sản chứa Flo như fluorit (CaF2).
CaF2 + H2SO4 → 2HF + CaSO4
- Flo được điều chế từ axit Flohydric (HF) thông qua các phản ứng hóa học phức tạp:
HF + H2O → H3O+ + F-
+ Phương pháp điện phân dung dịch muối Flo: Điện phân hỗn hợp KF trong HF lỏng khan đã được loại bỏ hết nước ở nhiệt độ 70 độ
Ứng dụng
– Ứng dụng điều chế một số dẫn xuất hiđrocacbon có chứa khí flo để sản xuất chất dẻo.
– (CF2-CFCl)n có chứa F dùng bảo vệ đồ dùng bằng kim loại, gốm sứ…tránh ăn mòn.
– Hợp chất của Flo sử dụng trong công nghệ điêu khắc, cắt thủy tinh.
– Teflon chứa F là polime dùng trong việc tạo ra các vòng đệm làm kín chân không, tạo bề mặt không dính cho các đồ dùng trong nhà
bếp.
– Hợp chất NaF nồng độ loãng làm thuốc chống sâu răng trong y học, sử dụng trong công nghiệp nghiên cứu hạt nhân.
Một số hợp chất
*Hợp chất của flo với oxi: OF2( oxi diflorua)
- Oxi diflorua là chất khí không màu, có mùi đặc biệt, rất độc.
- Là chất oxi hóa mạnh, tác dụng với hầu hết các kim loại và phi kim tạo thành oxit và florua.
- Trong hợp chất OF2, flo có số oxi hóa −1 và oxi có số oxi hóa +2.
- Điều chế: dẫn flo qua dung dịch NaOH loãng (khoảng 2%) khi làm lạnh nhanh.
*Hiđro florua và axit flohiđric: HF
- Axit flohiđric là axit yếu.
-Tính chất đặc biệt của axit flohiđric: tác dụng với silic đioxit (có trong thành phần của thủy tinh).
- Axit flohiđric được dùng để khắc chữ nổi lên thủy tinh.
- Muối của axit flohiđric là Bạc florua (AgF) dễ tan trong nước.
- Các muối florua đều độc.
- Điều chế hiđro florua: Cho canxi florua tác dụng với axit sunfuric đặc ở 50 độ C. Hiđro florua tan vô hạn trong nước tạo ra dung dịch
axit flohiđric.
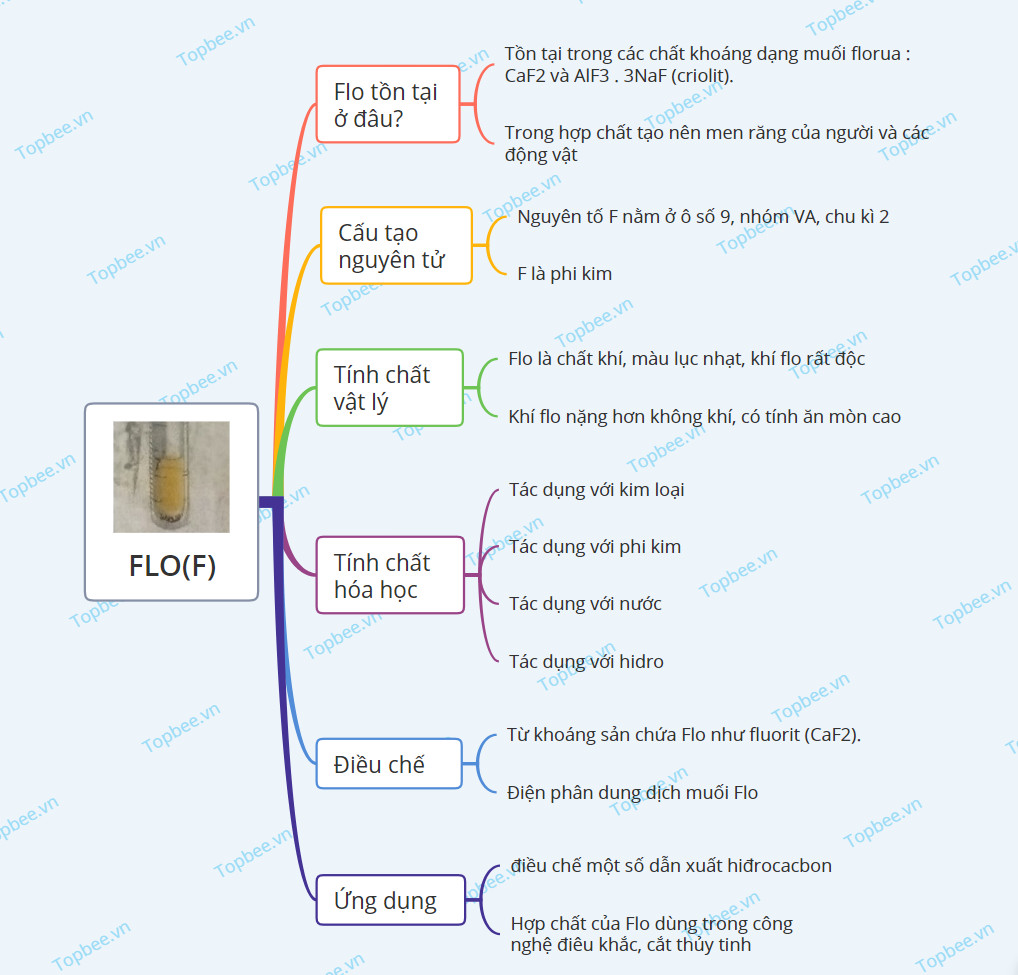
Sơ đồ tư duy về Flo
Một số câu hỏi về Flo và hợp chất của Flo
Câu 1: Trong hợp chất, nguyên tố Flo thể hiện số oxi hóa là
A. 0.
B. +1.
C. -1.
D. +3.
Câu 2: Nguyên nhân gây ra bệnh fluorosis (bệnh chết răng) là
A. nguồn thực phẩm bị nhiễm độc thuốc trừ sâu.
B. nguồn nước bị ô nhiễm flo.
C. nước thải có hợp chất chứa oxi của clo vượt quá mức cho phép.
D. người dân không sử dụng kem đánh răng.
Câu 3: Dung dịch axit nào sau đây không thể chứa trong bình thủy tinh:
A. HCl.
B. H2SO4.
C. HNO3.
D. HF.
Câu 4: Tính khối lượng CaF2 cần dùng để điều chế 2,5kg dung dịch axit flohidric nồng độ 40%. Biết hiệu suất phản ứng là 80%.





