

K2CO3 + 2HBr → 2KBr + CO2 + H2O | Cân bằng PTHH Potassium carbonat
 27/6/2024
27/6/2024
Cân bằng PTHH: K2CO3 + 2HBr → 2KBr + CO2 + H2O chính xác và dễ hiểu nhất kèm theo bài tập vận dụng có đáp án chi tiết
1. Loại phản ứng
Phản ứng trao đổi
2. Cân bằng PTHH:
K2CO3 + 2HBr → 2KBr + CO2 + H2O
3. Điều kiện xảy ra phản ứng/ Xúc tác phản ứng
Điều kiện thường.
4. Cách tiến hành thí nghiệm
Nhỏ HBr vào ống nghiệm chứa K2CO3.
5. Chất tạo ra từ phản ứng:
- KBr là một hợp chất muối màu trắng, không mùi, có vị mặn đắng nhẹ.
- CO2 ở điều kiện bình thường tồn tại ở dạng khí không màu, không mùi, không vị trong khí quyển Trái Đất.
6. Hiện tượng quan sát từ phản ứng
Có khí không màu thoát ra.
7. Ứng dụng của PTHH trên
- Phương trình hóa học trên được dùng đểlàm lạnh, bảo quản thực phẩm, tạo ra nước soda và nhiều sản phẩm khác.
8. Bài tập vận dụng
Bài tập 1: Nhỏ HBr vào ống nghiệm chứa K2CO3 thu được hiện tượng là
A.Có khí không màu thoát ra.
B.Có khí màu nâu đỏ thoát ra.
C.Có khí màu vàng lục, mùi xốc thoát ra.
D.Không có hiện tượng gì.
Lời giải
K2CO3 + 2HBr → 2KBr + CO2 + H2O
CO2: khí không màu,
Đáp án A.
Bài tập 2: Thể tích khí ở dktc thoát ra khi cho 13,8g K2CO3 phản ứng hoàn toàn với lượng dư HBr là
A.1,12 lít.B. 2,24 lít.C. 3,36 lít.D. 4,48 lít.
Lời giải
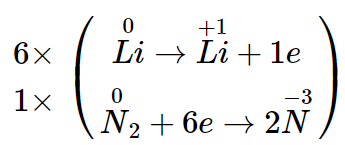
V = 0,1.22,4 = 2,24 lít.
Đáp án B.
Bài tập 3: Cho 1,38g K2CO3 phản ứng hoàn toàn với lượng HBr, khối lượng muối có trong dung dịch thu được sau phản ứng là
A.2,38 gam.B, 0,745 gam.C. 0,475 gam.D. 1,49 gam.
Lời giải
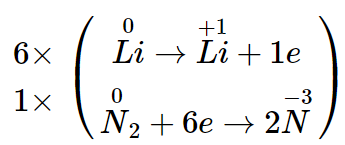
khối lượng muối = 0,02.119 = 2,38 gam.
Đáp án A.





