Na2CO3 (kết tủa không, điện ly mạnh hay yếu, mindmap)
 13/1/2024
13/1/2024
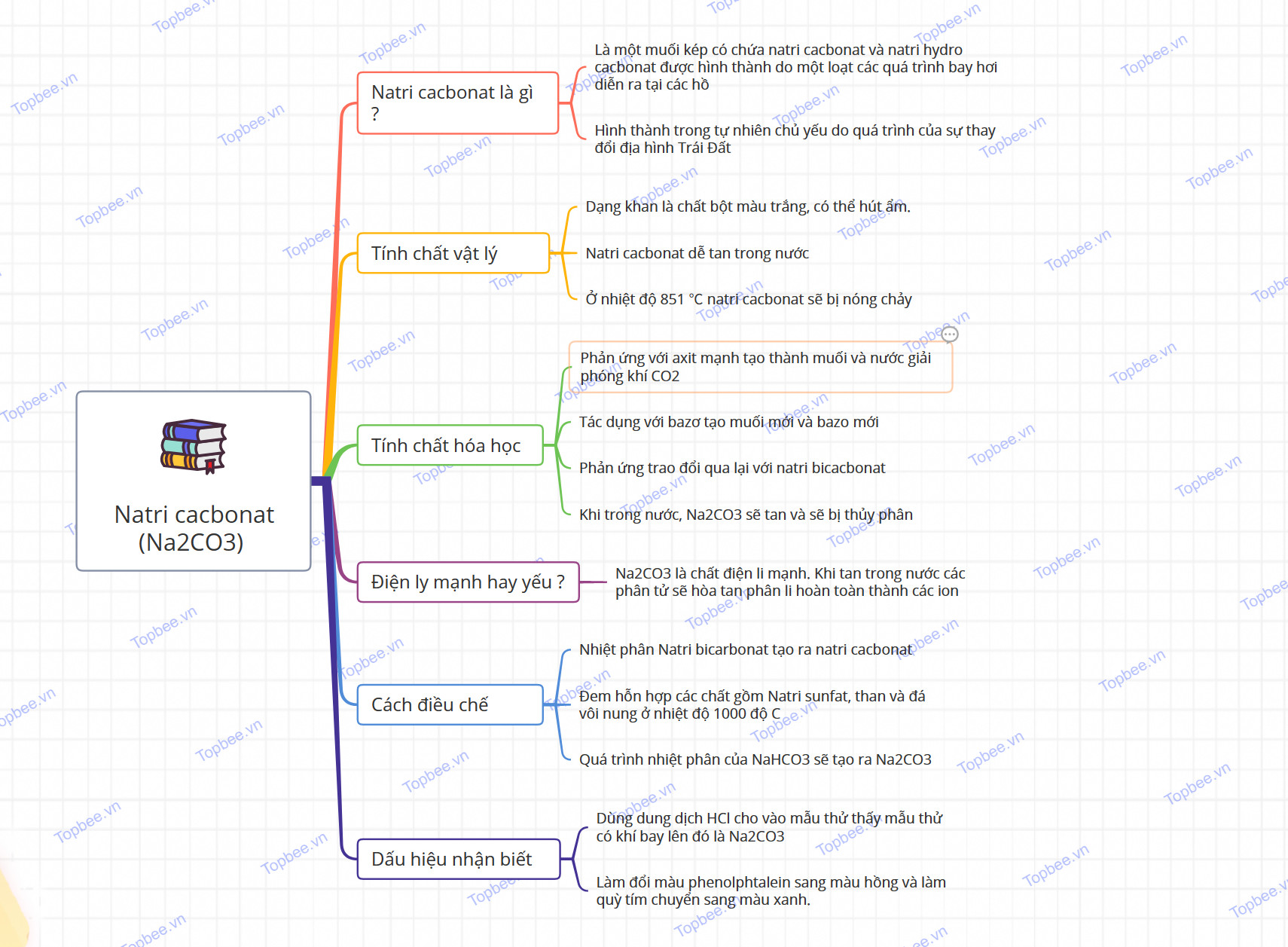
Tổng hợp kiến thức về Na2CO3: Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức
Natri cacbonat (Na2CO3) là gì ?
- Khái niệm: Natri cacbonat là một muối kép có chứa natri cacbonat và natri hydro cacbonat được hình thành do một loạt các quá trình bay hơi diễn ra tại các hồ. Có công thức hóa học được ký hiệu là Na2CO3
- Nó được biết đến với các tên gọi là tinh thể Soda, tro soda, soda rửa.
- Cấu tạo phân tử:
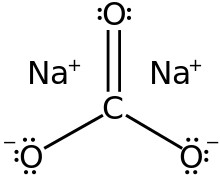
- Natri cacbonat là một muối bền trong tự nhiên, thường có trong nước khoáng, nước biển và muối mỏ trong lòng đất. Một số ít tồn tại ở dạng tinh thể có lẫn Canxi Cacbonat.
- Hình thành trong tự nhiên chủ yếu do quá trình của sự thay đổi địa hình Trái Đất làm một số hồ gần biển hoặc vịnh bị khép kín, dần dần lượng muối tích tụ lại và bị chôn vùi vào lòng đất tạo thành mỏ muối. Còn lại trong tự nhiên là lượng muối của nước biển được hình thành do hòa tan khí CO2 trong không khí.
Tính chất vật lý
- Na2CO3 khan là chất bột màu trắng, có thể hút ẩm.
- Natri cacbonat dễ tan trong nước:
+ Dưới nhiệt độ 32,5ºC kết tinh thành Na2CO3.10H2
+ Trong khoảng 32,5-37,5 ºC tạo thành chất Na2CO3.7H2O
+ Trên 37,5 ºC thành Na2CO3.H2O
+ Đến 107 ºC mất nước thành Na2CO3 khan.
- Ở nhiệt độ 851 ℃ natri cacbonat sẽ bị nóng chảy nếu cao hơn nhiệt độ 853 ℃ thì bắt đầu phân hủy.
Tính chất hóa học
- Na2CO3 là chất lưỡng tính tác dụng được cả axit và bazơ.
- Phản ứng với axit mạnh tạo thành muối và nước giải phóng khí CO2:
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
-Tác dụng với bazơ tạo muối mới và bazo mới:
Na2CO3 + Ca(OH)2 → 2NaOH + CaCO3↓
- Tác dụng với muối tạo hai muối mới:
Na2CO3 + CaCl2 → 2NaCl + CaCO3
- Phản ứng trao đổi qua lại với natri bicacbonat như phương trình sau:
Na2CO3 + CO2 + H2O ⇌ 2NaHCO3
- Khi trong nước, Na2CO3 sẽ tan và sẽ bị thủy phân:
Na2CO3 → 2Na+ + CO32−
CO32− + H2O ⇌ HCO3− + OH− ⇒ Dung dịch Na2CO3 có tính bazo yếu.
- Na2CO3 làm đổi màu các chất chỉ thị dung dịch phenolphtalein không màu chuyển sang màu hồng và làm quỳ tím chuyển sang màu xanh.
Natri cacbonat (Na2CO3) là chất điện ly mạnh hay yếu ?
- Na2CO3 là chất điện li mạnh. Khi tan trong nước các phân tử sẽ hòa tan phân li hoàn toàn thành các ion.
Natri cacbonat (Na2CO3) có kết tủa không ?
- Na2CO3 là một muối natri không kết tủa. Trong điều kiện thường, Na2CO3 khan là chất bột màu trắng, mùi nồng. Nhưng khi để lâu trong không khí, thì Na2CO3 xuất hiện hiện tượng chảy nước.
PTHH thường gặp
Na2CO3 + CaCl2 → CaCO3 + 2NaCl
CaCO3 + Na2CO3 + 6SiO2 → 2CO2 + Na2O.CaO.SiO2
3Na2CO3 + 2FeCl3 → Fe2(CO3)3 + 6NaCl
2HNO3 + Na2CO3 → H2O + 2NaNO3 + CO2
NaCO3 + Mg(HCO3)2 → MgCO3 + 2NaHCO3
Phương pháp điều chế
- Nhiệt phân Natri bicarbonat tạo ra natri cacbonat:
2NaHCO3 →Na2CO3 + CO2 + H2O
- Đem hỗn hợp các chất gồm Natri sunfat, than và đá vôi nung ở nhiệt độ 1000 độ C.
Na2SO4 + 2C → Na2S + 2CO2
Na2S + CaCO3 → Na2CO3 + CaS
- Sản phẩm tạo nhờ vào quá trình nhiệt phân của NaHCO3 sẽ tạo ra Na2CO3.
2NaHCO3 ↔ Na2CO3 + CO2(k) + H2O
Dấu hiệu nhận biết
- Dùng dung dịch HCl cho vào mẫu thử thấy mẫu thử có khí bay lên đó là Na2CO3:
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑
- Na2CO3 làm đổi màu các chất chỉ thị dung dịch phenolphtalein không màu chuyển sang màu hồng và làm quỳ tím chuyển sang màu xanh.
Sơ đồ tư duy của Natri cacbonat (Na2CO3)