NaCl (kết tủa không, điện ly mạnh hay yếu, mindmap)
 11/1/2024
11/1/2024
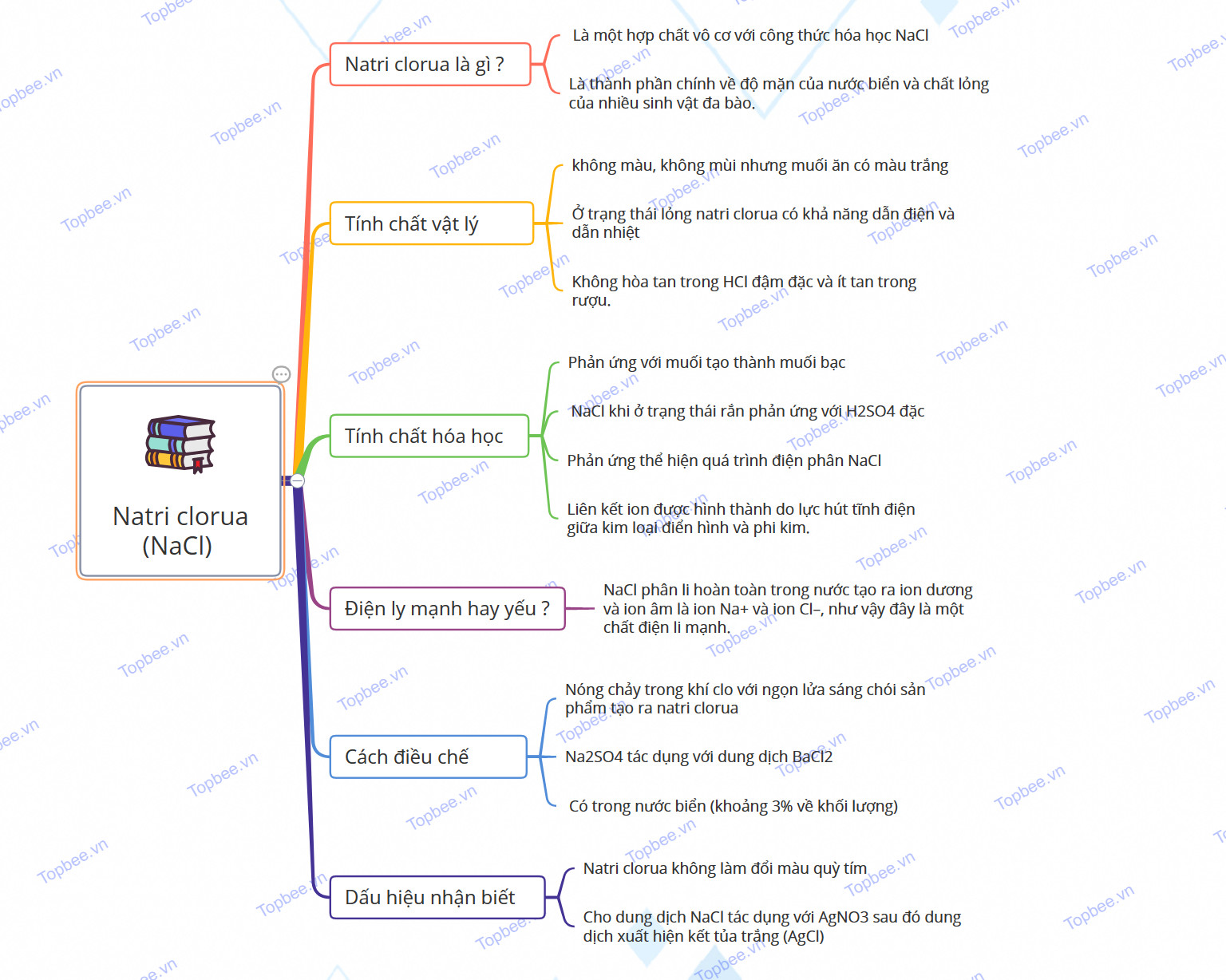
Tổng hợp kiến thức về NaCl: Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức
Natri clorua (NaCl) là gì ?
- Khái niệm: Natri clorua là một hợp chất vô cơ với công thức hóa học NaCl. Còn được gọi là muối ăn, muối tinh khiết, muối mỏ hoặc muối halogenua.
- Cấu tạo phân tử:
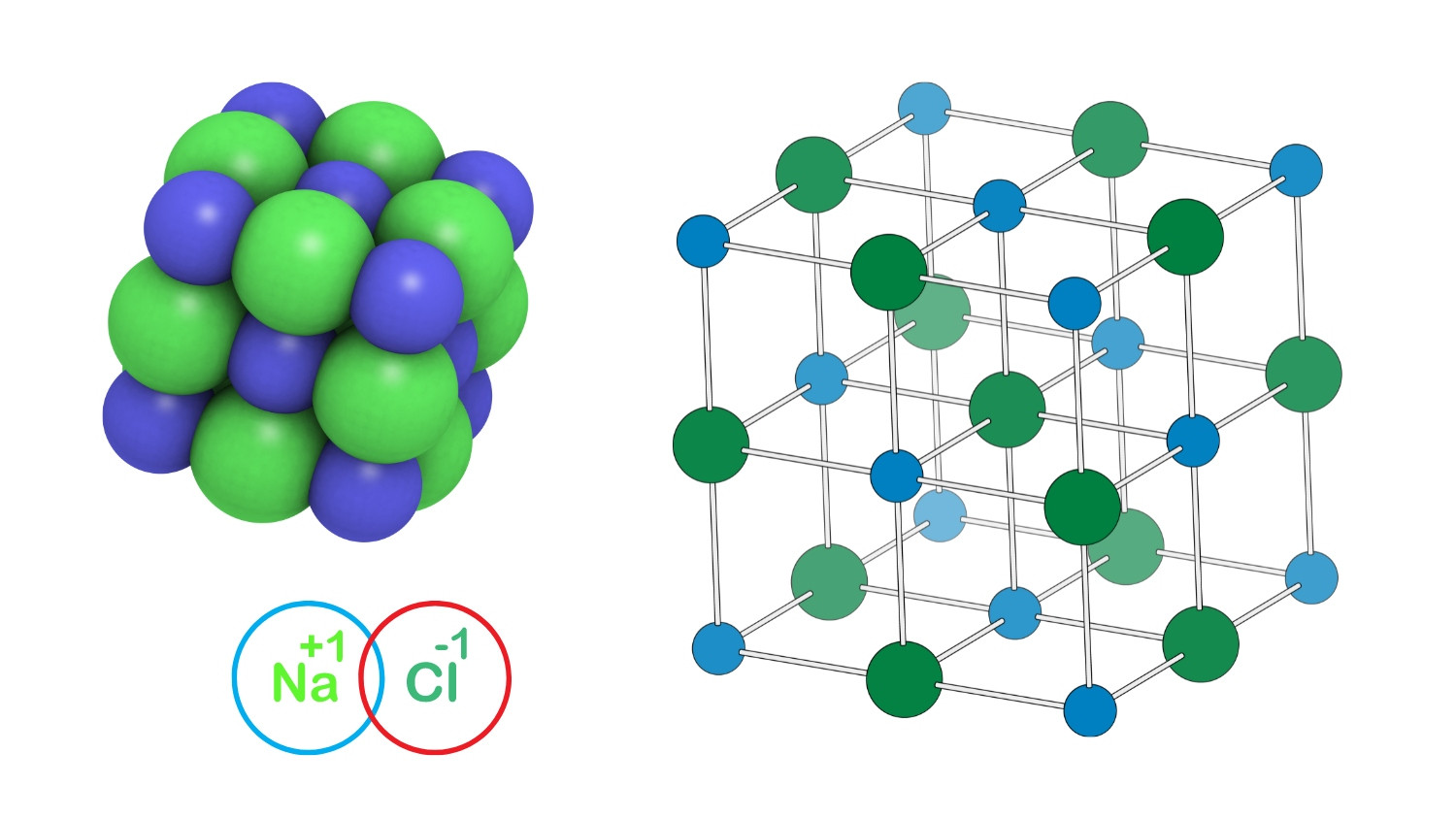
- NaCl là thành phần chính về độ mặn của nước biển và chất lỏng của nhiều sinh vật đa bào.
- Ngoài ra nó còn có ở các miệng núi lửa hoặc đá dưới đáy biển. Tuy nhiên, hầu hết muối có nguồn gốc trên cạn: nước ngọt từ mưa không phải là 100% tinh khiết, nó giải phóng CO2 từ khí quyển và rơi xuống đất.
Tính chất vật lý
- Do có MgCl2 và CaCl2 cho nên NaCl không màu, không mùi nhưng muối ăn có màu trắng
- Nhiệt độ nóng chảy của muối NaCl rất cao, ở 801 độ C và bắt đầu bốc hơi ở nhiệt độ ngay trên điểm sôi 1413 độ C.
- Độ tan của muối NaCl ở trong dung dịch giảm xuống khi các chất như NaOH, CaCl2, HCl, MgCl2
- Khi ở trạng thái lỏng và dung dịch muối natri clorua có khả năng dẫn điện và dẫn nhiệt nhưng không thể khi tồn tại ở trạng thái rắn.
- Không hòa tan trong axit clohydric (HCl) đậm đặc và ít tan trong rượu.
- Nhiệt độ nóng chảy: 801 độ C
- Nhiệt độ sôi: 1465°C
- Nguyên tử khối: 58,4 g/mol
Tính chất hóa học
- NaCl là loại muối trung hòa mà anion axit không có khả năng phân ly thành ion H+. Có độ pH = 7 không làm đổi màu quỳ tím.
- Liên kết ion được hình thành do lực hút tĩnh điện giữa kim loại điển hình và phi kim.
- Khi cho HCl đậm đặc vào dung dịch natri clorua bão hòa thì xuất hiện kết tủa trắng. Khi thêm nước vào hỗn hợp này, kết tủa sẽ tan trở lại.
- Phản ứng với muối tạo thành muối bạc, cụ thể như sau:
AgNO3 + NaCl → AgCl + NaNO3
- Muối NaCl khi ở trạng thái rắn phản ứng với H2SO4 đặc, ta có phương trình phản ứng sau:
NaCl + H2SO4 → NaHSO4 + HCl
- Phản ứng thể hiện quá trình điện phân NaCl là:
2NaCl + 2H2O → 2NaOH + H2 + Cl2
Natri clorua là chất điện ly mạnh hay yếu ?
- NaCl phân li hoàn toàn trong nước tạo ra ion dương và ion âm là ion Na+ và ion Cl–, như vậy đây là một chất điện li mạnh.
Natri clorua có kết tủa không ?
- NaCl có kết tủa không phụ thuộc vào hợp chất mà nó kết hợp. Nếu dung dịch này là nước tinh khiết, NaCl sẽ kết tủa màu trắng giống màu của NaCl khi ở trạng thái rắn.
PTHH thường gặp
2NaCl + 2H2O → 2NaOH + Cl2↑ + H2↑
NaCl + AgNO3 → NaNO3 + AgCl↓
NaCl + H2SO4 → NaHSO4 + HCl ↑ ( điều kiện phản ứng là 250 độ C)
2NaCl + H2SO4 → Na2SO4 + 2HCl ↑ ( điều kiện phản ứng là 400 độ C)
Phương pháp điều chế
- Natri nóng chảy trong khí clo với ngọn lửa sáng chói sản phẩm tạo ra natri clorua, như phương trình dưới đây:
Cl2 + 2Na → 2NaCl ( Điều kiện nhiệt độ)
- Nhỏ vài giọt dung dịch phenolphtalein vào cốc đựng dung dịch NaOH 0,10M, dung dịch có màu hồng. Rót từ từ dung dịch HCl 0,10M vào cốc trên, vừa rót vừa khuấy:
HCl + NaOH → H2O + NaCl
Cho Na2SO4 tác dụng với dung dịch BaCl2 sau đó xuất hiện kết tủa trắng BaSO4 trong dung dịch như sau:
BaCl2 + Na2SO4 → 2NaCl + BaSO4
- Ngoài ra nó còn có trong nước biển (khoảng 3% về khối lượng), nước của hồ nước mặn và trong khoáng vật halit (gọi là muối mỏ).
Dấu hiệu nhận biết
- Natri clorua không làm đổi màu quỳ tím
- Cho dung dịch NaCl tác dụng với AgNO3 sau đó dung dịch xuất hiện kết tủa trắng (AgCl)
Sơ đồ tư duy của Natri clorua