NaHCO3 (kết tủa không, điện ly mạnh hay yếu, mindmap)
 13/1/2024
13/1/2024
Tổng hợp kiến thức về NaHCO3: Cấu tạo phân tử, Tính chất vật lí, hóa học, phương pháp điều chế, ứng dụng, Mindmap giúp học sinh ôn tập, bổ sung kiến thức
Natri bicarbonat (NaHCO3) là gì ?
- Khái niệm: Natri bicarbonat là một hợp chất vô cơ và có công thức hóa học ký hiệu là NaHCO3.
- NaHCO3 có vị hơi mặn và có tính kiềm tương tự như loại soda dùng trong tẩy rửa.
- Vì hiện nay được sử dụng rất phổ biến trong thực phẩm nên nó được nhiều biết đến với các tên gọi khác nhua như: cooking soda, bicarbonate of soda, bread soda,…
Tính chất vật lý
- Natri bicarbonat là chất rắn màu trắng và có dạng tinh thể đơn, tồn tại dưới dạng giống như bột, có vị hơi mặn và có tính kiềm giống như loại soda dùng trong tẩy rửa.
- NaHCO3 ít tan trong nước và gần như không tan.
- Ở nhiệt độ 50oC NaHCO3 sẽ bị phân hủy
- Khối lượng mol là 84,007 g/mol
- Khối lượng riêng là 2,159 g/cm3
- Độ hòa tan trong nước: 7,8 g/100ml (18 oC)
Tính chất hóa học
- Phản ứng với bazơ tạo muối mới và bazơ mới:
NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O
- Hoặc cũng có thể tạo ra hai muối mới:
2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O
- Trong dung dịch nước NaHCO3 sẽ bị thủy phân tạo thành môi trường bazơ yếu có thể đổi màu quỳ tím:
NaHCO3 + H2O → NaOH + H2CO3
- Phản ứng với axit mạnh tạo thành muối và nước đồng thời giải phóng khí CO2:
2NaHCO3 + H2SO4 → Na2SO4 + 2H2O + 2CO2
- Tác dụng với NaOH tạo ra muối trung hòa và nước:
NaHCO3 + NaOH → Na2CO3 + H2O
Natri bicarbonat (NaHCO3) là chất điện ly mạnh hay yếu ?
- Khi tan trong nước NaHCO3 các phân tử hòa tan và phân li hoàn toàn vì vậy NaHCO3 là chất điện ly mạnh.
Natri bicarbonat (NaHCO3) có kết tủa không ?
- Natri bicarbonat tác dụng với bazo sẽ có hiện tượng kết tủa trắng:
NaHCO3 + Ca(OH)2→ CaCO3 ↓ + NaOH + H2O
PTHH thường gặp
NaHCO3 + HCl → NaCl + H2O + CO2
2NaHCO3 + Ba(OH)2 → BaCO3 + Na2CO3 + 2H2O
NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O
15CH3COOH + 10NaHCO3 → 10CH3COONa + 2H20 + 20CO2
2NaHCO3 + BaCl2 → 2NaCl + CO2 + BaCO3 + H2O
Phương pháp điều chế
- NaHCO3 thường sẽ được sản xuất bằng cách cho các chất canxi cacbonat cùng natri clorua và amoiac phản ứng với nhau.
- Cho cacbon dioxit tác dụng với natri hidroxit, sau đó thêm CO2 dư tạo ra NaHCO3, sau đó đem đi cô đặc dung dịch thu được muối ở dạng khan, cụ thể như quá trình phản ứng sau:
CO2 + 2NaOH → Na2CO3 + H2O
Na2CO3 + CO2 + H2O → 2NaHCO3
- NaHCO3 ccòn có thể tìm thấy trong tự nhiên như trong các quặng nahcolite tại những nơi có suối khoáng.
Dấu hiệu nhận biết
- Chúng ta thể thử cho NaHCO3 bằng giấy pH vào trên khí CO2, giấy pH sẽ chuyển màu từ màu xanh lam sang màu đỏ.
- Cho tác dụng với dung dịch muối bạc nitrat (AgNO3), sẽ có hiện tượng kết tủa trắng của AgHCO3.
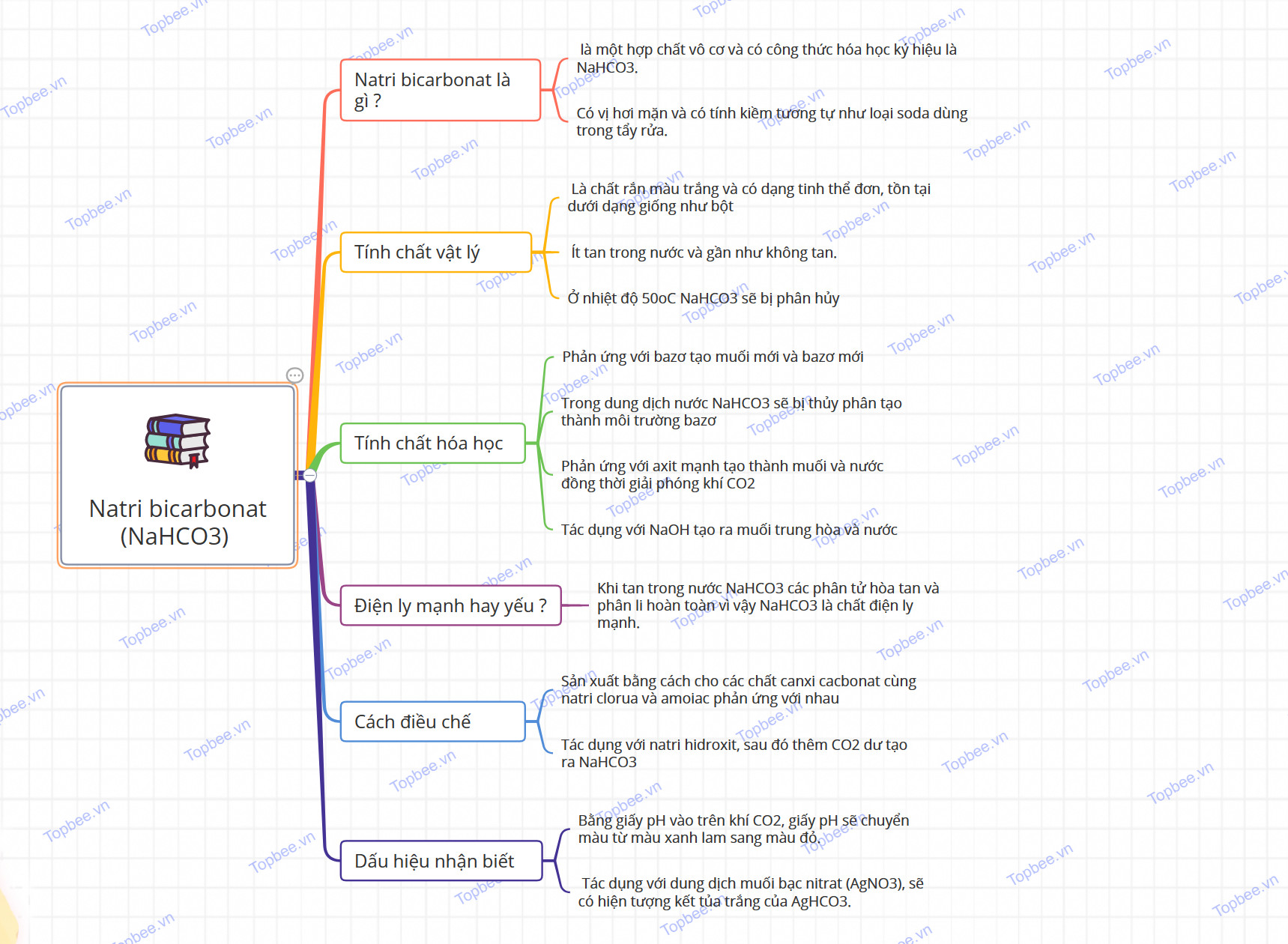
Sơ đồ tư duy của Natri bicarbonat (NaHCO3)