

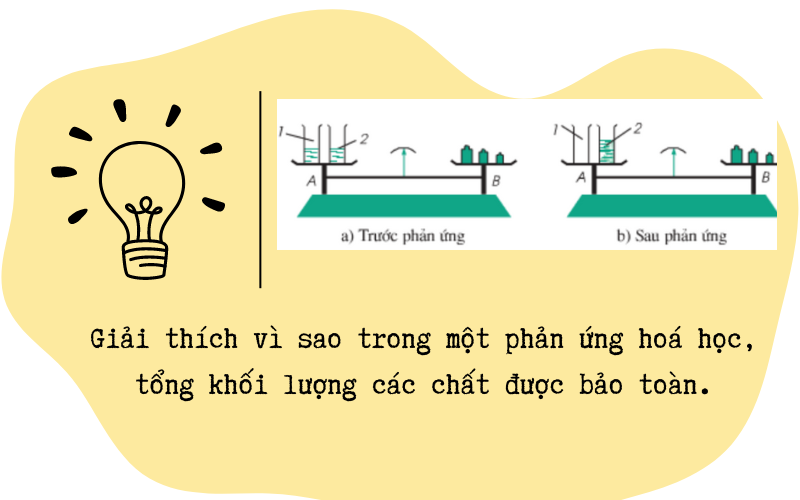
Giải thích vì sao trong một phản ứng hóa học, tổng khối lượng các chất tham gia được bảo toàn
 21/6/2023
21/6/2023
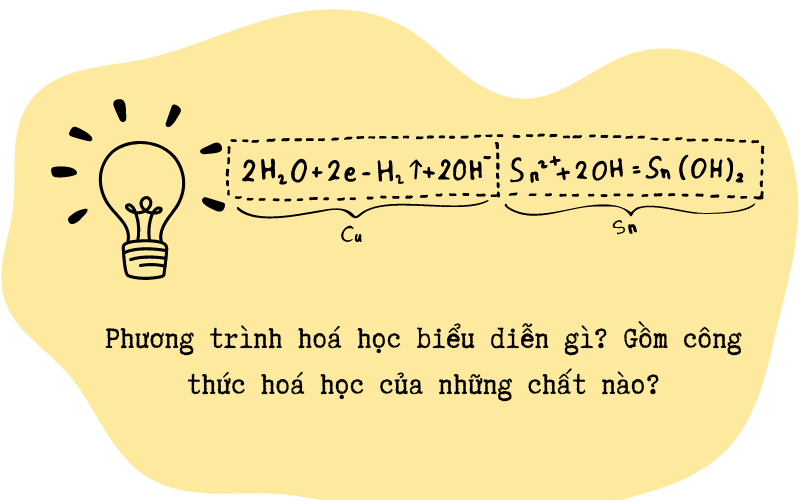
Hướng dẫn Trả lời câu hỏi Khoa học tự nhiên 8 trang 24 Chân trời sáng tạo: Giải thích vì sao trong một phản ứng hoá học, tổng khối lượng các chất được bảo toàn. Phương trình hoá học biểu diễn gì? Gồm công thức hoá học của những chất nào?
Luyện tập trang 24 Khoa học tự nhiên 8
Trả lời:
Theo mô hình nguyên tử, các chất tham gia phản ứng và các chất sản phẩm đều được tạo thành từ các nguyên tử. Trong quá trình phản ứng hóa học, các liên kết giữa các nguyên tử thay đổi, nhưng số lượng nguyên tử không thay đổi.
Ví dụ, khi xảy ra phản ứng đốt cháy hoàn toàn một khối lượng dầu mỏ, khí oxi (O2) từ không khí sẽ tác động lên dầu mỏ để tạo ra khí cacbon điôxít (CO2) và nước (H2O). Trong quá trình này, tổng khối lượng của dầu mỏ, khí oxi và các sản phẩm CO2 và H2O sẽ không thay đổi. Tất cả các nguyên tử cacbon và ôxi trong dầu mỏ và khí oxi sẽ được tái sắp xếp để tạo thành các phân tử CO2 và H2O, nhưng tổng số nguyên tử của các nguyên tố này không thay đổi.
Câu hỏi thảo luận 4 trang 24 Khoa học tự nhiên 8
Trả lời:
Phương trình hoá học biểu diễn phản ứng hoá học. Gồm công thức hoá học của chất phản ứng và chất sản phẩm.
Phương trình hóa học là một cách biểu diễn phản ứng hóa học bằng các ký hiệu hóa học và số lượng tương ứng của các chất tham gia và sản phẩm. Phương trình hóa học giúp mô tả cách các chất tham gia tương tác với nhau để tạo ra các chất mới.
Một phương trình hóa học có thể có dạng như sau:
Chất tham gia + Chất tham gia → Sản phẩm + Sản phẩm
Ví dụ, phản ứng đốt cháy hydro (H2) trong không khí (O2) để tạo ra nước (H2O) có thể được biểu diễn bằng phương trình hóa học như sau:
2H2 + O2 → 2H2O
Trong phương trình này, các chất tham gia là H2 và O2, và sản phẩm là H2O. Con số bên trước các chất hóa học được gọi là hệ số stoichiometric, thể hiện tỷ lệ số lượng mol giữa các chất tham gia và sản phẩm trong phản ứng. Trong ví dụ trên, với hệ số stoichiometric là 2, nghĩa là cần 2 phân tử H2 và 1 phân tử O2 để tạo ra 2 phân tử H2O.
Phương trình hóa học cũng có thể bao gồm các điều kiện phản ứng như nhiệt độ, áp suất, xúc tác, được đặt bên dưới phản ứng. Ví dụ, phản ứng đốt cháy trên có thể được viết lại kèm theo điều kiện như sau:
2H2 + O2 → 2H2O + nhiệt





