

Kali | K (CTCT, Tính chất vật lí, hóa học, Điều chế, Mindmap)
 26/12/2023
26/12/2023
Bài viết tìm hiểu về Kali (K) do Topbee biên soạn tổng hợp kiến thức trọng tâm về Kali (K): Công thức hóa học, Tính chất vật lí, hóa học, Điều chế, Mindmap giúp học sinh ôn tập và bổ sung kiến thức cũng như hoàn thành tốt các bài kiểm tra môn Hóa học.
Kali tồn tại ở đâu?
- Kali là nguyên tố hóa học có ký hiệu hóa học là K và số hiệu nguyên tử là 19 trong bảng tuần hoàn hóa học.
- Nguyên tố này chiếm khoảng 2,4% trọng lượng lớp vỏ Trái Đất.
- Trong tự nhiên, Kali tồn tại dưới dạng muối ion
+ K được phát hiện ở dạng hòa tan trong nước biển(0,04% K)
+ Tồn tại trong các khoáng vật: Granit chứa 5% K, xinvinit(KCl), cacnalit(KCl.MgCl2.6(H2O)),..
Cấu tạo nguyên tử Kali
+ Cấu hình electron của K là: 1s22s22p63s23p64s1 hay [Ar]4s1
+ Nguyên tử K có 19 electron, chu kì 4, nhóm IA, cấu trúc mạng tinh thể lập phương tâm khối.
+ Là một kim loại điển hình trong nhóm kiềm thổ
+ Kali có 3 đồng vị: 39K(93,3%), 40K (0,01%) và 41K (6,7%).
+ K có xu hướng nhường 1 electron lớp ngoài cùng khi tham gia phản ứng hóa học để đạt cấu hình bền vững của Ar.
K ⟶ K+ + 1e
Tính chất vật lý
+ Kali là một chất rắn rất mềm, màu trắng bạc, có ánh kim.
+ Là kim loại kiềm có thể cắt được
+ Khối lượng riêng nhỏ hơn nước, Kali nhẹ thứ hai sau liti.
+ Nguyên tử khối: 39 g/mol
+ Trong không khí, K bị oxi hóa nhanh nên được bảo quản trong dầu mỏ hay dầu lửa.
+ Nhiệt độ nóng chảy: 336,53°K (63,38°C, 146,08°F)
+ Nhiệt độ sôi: 1032°K (759°C, 1398°F)
Tính chất hóa học
- K có tính khử rất mạnh.
a. Tác dụng với phi kim
4K + O2 → 2K2O
2K + Cl2 → 2KCl
- Khi đốt trong không khí hay trong oxi, kali cháy tạo thành các oxit (oxit thường, peoxit và supeoxit) và cho ngọn lửa có màu tím hoa cà
đặc trưng.
b. Tác dụng với axit
- Kali dễ dàng khử ion H+ (hay H3O+) trong dung dịch axit loãng (HCl, H2SO4 loãng...) thành hidro tự do.
2K + 2HCl → 2KCl + H2.
c. Tác dụng với nước
- K có tính háo nước vì vậy nó tác dụng mãnh liệt với nước và tự bùng cháy tạo thành dung dịch kiềm và giải phóng khí hidro.
2K + 2H2O → 2KOH + H2.
d. Tác dụng với hidro
- Kali tác dụng với hidro ở áp suất khá lớn và nhiệt độ khoảng 350 – 400oC tạo thành kali hidrua.
2K (lỏng) + H2 (khí) → 2KH (rắn)
Điều chế
Phương pháp điều chế: điện phân nóng chảy muối và bazơ của K là KCl:
2KCl → 2K + Cl2
Ứng dụng
+ Kali cân bằng lượng chất khoáng và nước mà cơ thể nhận và đào thải, giảm cao huyết áp,…
+ Kali nitrat được sử dụng trong thuốc súng; Kali cacbonat sử dụng trong sản xuất thủy tinh.
+ Ứng dụng trong ống phóng màn hình màu, đèn huỳnh quang, dệt nhuộm và chất tạo màu.
+ Hợp kim NaK là chất truyền nhiệt trung gian.
+ Sử dụng KOH làm bánh xà phòng từ mỡ và dầu trong công nghiệp tẩy rửa.
+ KCrO4 được dùng trong mực, nhuộm, chất tạo màu, trong chất nổ pháo hoa, diêm an toàn và giấy bẫy ruồi…
+ Kali là nguyên liệu sản xuất phân bón NPK, kali sulfate (K2SO4), kali sodium (KNO3), kali chloride (KCl) …
Một số hợp chất
*Kali oxit: K2O
+ Là oxit dạng bột màu trắng nhạt, không mùi.
+ Ít được thấy trong tự nhiên do tính chất hóa học quá mạnh.
+ K2O có thể tác dụng với nước ở điều kiện thường tạo Kali hidroxit và phản ứng với nhiều hợp chất khác.
- Kali oxit là chất xúc tác để sản xuất các hợp chất hữu cơ, chất chống cháy, sản xuất thủy tinh, phân bón hóa học,..
*Kali cacbonat: K2CO3
+ Là chất rắn, màu trắng, có tính hút ẩm.
+ Dễ hòa tan trong nước tạo thành dung dịch kiềm mạnh, nhưng không tan trong ethanol.
+ K2CO3 trong ngành sản xuất gốm sứ thủy tinh, chất nổ, phân bón, sản xuất xà phòng, muối vô cơ, nhuộm len…
+ K2CO3 là chất hóa học chảy rửa, thường hiện diện trong dạng chất rắn ẩm hoặc ướt.
*Kali hidroxit: KOH
+ Là tinh màu trắng, mùi đặc trưng, có tính hút ẩm
+ Tan hoàn toàn trong nước, khi tan trong nước tỏa ra nhiều nhiệt lượng
+ KOH được ứng dụng trong sản xuất xà phòng, chất tẩy rửa, phân bón,..
+ Kali hidroxit là nguyên liệu của dầu diezel sinh học, nhuộm len, vải,…
*Kali sunfat: K2SO4.
+ Là một muối rắn kết tinh màu trắng, không cháy và hòa tan trong nước.
- Kali sunfat có tính axit , có khả năng ăn mòn kim loại.
- Được dùng để sản xuất phân bón.
+ Ngoài ra K2SO4 còn được sử dụng để sản xuất thủy tinh
Sơ đồ tư duy về Kali
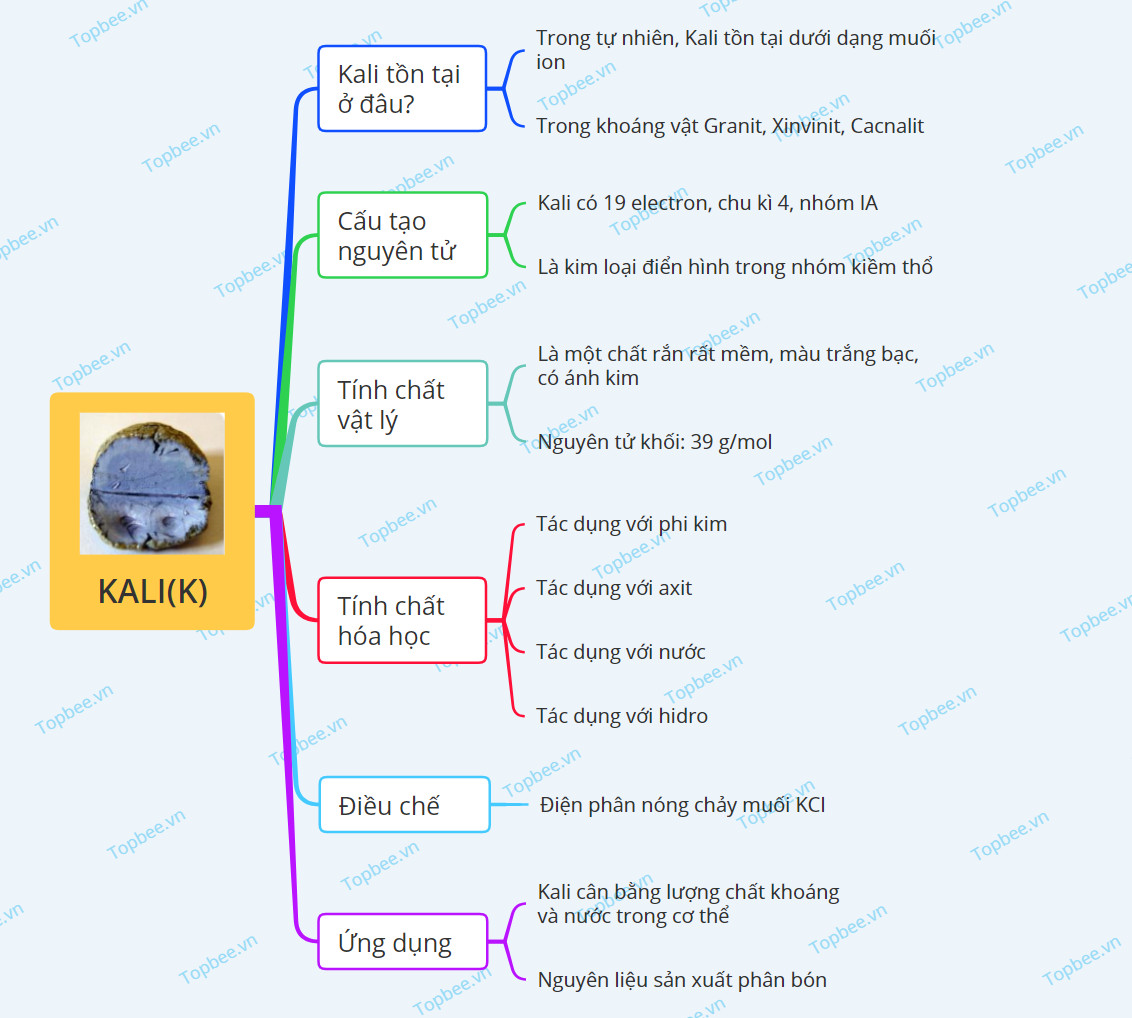
Một số câu hỏi về Kali và hợp chất của Kali
Câu 1: Cho K tác dụng với dung dịch brom dư thu được 1,19 g muối. Khối lượng K tham gia phản ứng là
A. 0,39 g
B. 3,9 g
C. 7,8 g
D. 0,78 g
Câu 2: Trong tự nhiên kali gồm ba đồng vị 39K chiếm 93,26% và đồng vị 40K chiếm 0,012% và đồng vị 41K. Brom là hỗn hợp hai đồng vị
79Br và 81Br với nguyên tử khối trung bình của brom là 79,92. Thành phần % khối lượng của 39K trong KBr là:
A. 30,56%
B. 29,92%
C. 31,03%
D. 30,55%
Câu 3: Để phân biệt một cách đơn giản nhất hợp chất của kali và hợp chất của natri ,người ta đưa các hợp chất của kalivà natri vào ngọn
lửa, những nguyên tố đó dễ ion hóa nhuốm màu ngọn lửa thành :
A. Tím của kali ,vàng của natri
B. B .Tím của natri ,vàng của kali
C. Đỏ của natri ,vàng của kali
D. D .Đỏ của kali,vàng của natri
Câu 4: Cho 7,8 g Kali tác dụng hết với oxi. Toàn bộ sản phẩm thu được đem hòa tan hết với nước thì thu được 160g dung dịch A. Tính
nồng độ phẩn trăm của dung dịch A.
A. 3,5%
B. 7%
C. 9%
D.14%
Câu 5: Cho m gam kim loại Kali tác dụng hoàn toàn với 1,12 (l) khí X2 (đktc) thì thu được 11,9 gam muối halogenua. Xác định công thức
của khí X2 và giá trị m
Một số phản ứng quan trọng của Kali và hợp chất Kali
Cân bằng PTHH Kai với các chất khác
Cân bằng PTHH K2CO3 với chất khác
Cân bằng PTHH K2O với chất khác
| III | Cân bằng PTHH K2O với chất khác | Hướng dẫn cân bằng |
| 1 | K2O + 2CH3COOH → 2CH3COOK + H2O | https://topbee.vn/blog/k2o-2ch3cooh-2ch3cook-h2o |
| 2 | K2O + 2HBr → 2KBr + H2O | https://topbee.vn/blog/k2o-2hbr-2kbr-h2o |
| 3 | K2O + 2HCl → 2KCl + H2O | https://topbee.vn/blog/k2o-2hcl-2kcl-h2o |
| 4 | K2O + 2HI → 2KI + H2O | https://topbee.vn/blog/k2o-2hi-2ki-h2o |
| 5 | K2O + 2HNO3 → 2KNO3 + H2O | https://topbee.vn/blog/k2o-2hno3-2kno3-h2o |
| 6 | K2O + CO2 → K2CO3 (to) | https://topbee.vn/blog/k2o-co2-k2co3 |
| 7 | K2O + H2O → 2KOH | https://topbee.vn/blog/k2o-h2o-2koh |
| 8 | K2O + H2SO4 → K2SO4 + H2O | https://topbee.vn/blog/k2o-h2so4-k2so4-h2o |
| 9 | K2O + SO2 → K2SO3 (to) | https://topbee.vn/blog/k2o-so2-k2so3 |
Cân bằng PTHH K2S với chất khác
| IV | Cân bằng PTHH K2S với chất khác | Hướng dẫn cân bằng |
| 1 | K2S + 2HBr → 2KBr + H2S | https://topbee.vn/blog/k2s-2hbr-2kbr-h2s |
| 2 | K2S + 2HCl → 2KCl + H2S | https://topbee.vn/blog/k2s-2hcl-2kcl-h2s |
| 3 | 3K2S + 8HNO3 → 3K2SO4 +8 NO + 4H2O | https://topbee.vn/blog/3k2s-8hno3-3k2so4-8-no-4h2o |
| 4 | K2S + Cu(NO3)2 → CuS ↓ + 2KNO3 | https://topbee.vn/blog/k2s-cuno32-cus-2kno3 |
| 5 | K2S + CuCl2 → CuS ↓ + 2KCl | https://topbee.vn/blog/k2s-cucl2-cus-2kcl |
| 6 | K2S + FeCl2 → FeS ↓ + 2KCl | https://topbee.vn/blog/k2s-fecl2-fes-2kcl |
| 7 | K2S + H2SO4 → K2SO4 + H2S | https://topbee.vn/blog/k2s-h2so4-k2so4-h2s |
| 8 | K2S + Pb(NO3)2 → PbS ↓ + 2KNO3 | https://topbee.vn/blog/k2s-pbno32-pbs-2kno3 |
| 9 | K2S + Zn(NO3)2 → ZnS ↓ + 2KNO3 | https://topbee.vn/blog/k2s-znno32-zns-2kno3 |
| 10 | K2S + ZnCl2 → ZnS ↓ + 2KCl | https://topbee.vn/blog/k2s-zncl2-zns-2kcl |
Cân bằng PTHH K2SO3 với chất khác
| V | Cân bằng PTHH K2SO3 với chất khác | Hướng dẫn cân bằng |
| 1 | K2SO3 + 2HCl → 2KCl + SO2 + H2O | https://topbee.vn/blog/k2so3-2hcl-2kcl-so2-h2o |
| 2 | 5K2SO3 + 2KMnO4 + 6KHSO4 → 9K2SO4 +2MnSO4 +3H2O | https://topbee.vn/blog/5k2so3-2kmno4-6khso4-9k2so4-2mnso4-3h2o |
| 3 | K2SO3 + Ba(NO3)2 → 2KNO3 + BaSO3( ↓) | https://topbee.vn/blog/k2so3-bano32-2kno3-baso3 |
| 4 | K2SO3 + Ba(OH)2 → 2KOH + BaSO3( ↓) | https://topbee.vn/blog/k2so3-baoh2-2koh-baso3 |
| 5 | K2SO3 + BaCl2 → 2KCl + BaSO3( ↓) | https://topbee.vn/blog/k2so3-bacl2-2kcl-baso3 |
| 6 | K2SO3 + Ca(NO3)2 → 2KNO3 + CaSO3( ↓) | https://topbee.vn/blog/k2so3-cano32-2kno3-caso3 |
| 7 | K2SO3 + Ca(OH)2 → 2KOH + CaSO3( ↓) | https://topbee.vn/blog/k2so3-caoh2-2koh-caso3 |
| 8 | K2SO3 + CaCl2 → 2KCl + CaSO3( ↓) | https://topbee.vn/blog/k2so3-cacl2-2kcl-caso3 |
| 9 | K2SO3 + H2SO4 → K2SO4 + SO2 + H2O | https://topbee.vn/blog/k2so3-h2so4-k2so4-so2-h2o |
| 10 | K2SO3 + SO2 + H2O → 2KHSO3 | https://topbee.vn/blog/k2so3-so2-h2o-2khso3 |
Cân bằng PTHH KHCO3 với chất khác
| VI | Cân bằng PTHH KHCO3 với chất khác | Hướng dẫn cân bằng |
| 1 | 2KHCO3 + 2NaHSO4 → K2SO4 + Na2SO4+ 2CO2 + 2H2O | https://topbee.vn/blog/2khco3-2nahso4-k2so4-na2so4-2co2-2h2o |
| 2 | 2KHCO3 + Ba(HSO4)2 → K2SO4 + BaSO4+ 2CO2 + 2H2O | https://topbee.vn/blog/2khco3-bahso42-k2so4-baso4-2co2-2h2o |
| 3 | 2KHCO3 + Ca(HSO4)2 → K2SO4 + CaSO4+ 2CO2 + 2H2O | https://topbee.vn/blog/2khco3-cahso42-k2so4-caso4-2co2-2h2o |
| 4 | 2KHCO3 + H2SO4 → K2SO4 + 2CO2 + 2H2O | https://topbee.vn/blog/2khco3-h2so4-k2so4-2co2-2h2o |
| 5 | KHCO3 + HBr → KBr + CO2 + H2O | https://topbee.vn/blog/khco3-hbr-kbr-co2-h2o |
| 6 | KHCO3 + HCl → KCl + CO2 + H2O | https://topbee.vn/blog/khco3-hcl-kcl-co2-h2o |
| 7 | KHCO3 + HNO3 → KNO3 + CO2 + H2O | https://topbee.vn/blog/khco3-hno3-kno3-co2-h2o |
| 8 | KHCO3 + KHSO4 → K2SO4 + CO2 + H2O | https://topbee.vn/blog/khco3-khso4-k2so4-co2-h2o |
| 9 | 2KHCO3 → K2CO3 +CO2 + H2O (to) | https://topbee.vn/blog/2khco3-k2co3-co2-h2o-to |
Cân bằng PTHH KHSO3 với chất khác
| VII | Cân bằng PTHH KHSO3 với chất khác | Hướng dẫn cân bằng |
| 1 | 2KHSO3 + 2NaHSO4 → K2SO4 + Na2SO4+ 2SO2 + 2H2O | https://topbee.vn/blog/2khso3-2nahso4-k2so4-na2so4-2so2-2h2o |
| 2 | 2KHSO3 + Ba(HSO4)2 → K2SO4 + BaSO4+ 2SO2 + 2H2O | https://topbee.vn/blog/2khso3-bahso42-k2so4-baso4-2so2-2h2o |
| 3 | 2KHSO3 + Ca(HSO4)2 → K2SO4 + CaSO4+ 2SO2 + 2H2O | https://topbee.vn/blog/2khso3-cahso42-k2so4-caso4-2so2-2h2o |
| 4 | 2KHSO3 + H2SO4 → K2SO4 + 2SO2 + 2H2O | https://topbee.vn/blog/2khso3-h2so4-k2so4-2so2-2h2o |
| 5 | KHSO3 + HBr → KBr + SO2 + H2O | https://topbee.vn/blog/khso3-hbr-kbr-so2-h2o |
| 6 | KHSO3 + HCl → KCl + SO2 + H2O | https://topbee.vn/blog/khso3-hcl-kcl-so2-h2o |
| 7 | KHSO3 + KHSO4 → K2SO4 + SO2 + H2O | https://topbee.vn/blog/khso3-khso4-k2so4-so2-h2o |
| 8 | 2KHSO3 → K2SO3 +SO2 + H2O (to) | https://topbee.vn/blog/2khso3-k2so3-so2-h2o |
Cân bằng PTHH KI với chất khác
| VIII | Cân bằng PTHH KI với chất khác | Hướng dẫn cân bằng |
| 1 | 2KI + 2Fe(NO3)3 → I2 + 2Fe(NO3)2 + 2KNO3 | https://topbee.vn/blog/2ki-2feno33-i2-2feno32-2kno3 |
| 2 | 2KI + 2FeCl3 → I2 + 2FeCl2 + 2KCl | https://topbee.vn/blog/2ki-2fecl3-i2-2fecl2-2kcl |
| 3 | KI + AgNO3 → KNO3 + AgI ( ↓) | https://topbee.vn/blog/ki-agno3-kno3-agi |
| 4 | 2KI + Br2 → 2KBr + I2 | https://topbee.vn/blog/2ki-br2-2kbr-i2 |
| 5 | 2KI + Cl2 → 2KCl + I2 | https://topbee.vn/blog/2ki-cl2-2kcl-i2 |
| 6 | 2KI + Fe2(SO4)3 → I2 + 2FeSO4 + K2SO4 | https://topbee.vn/blog/2ki-fe2so43-i2-2feso4-k2so4 |
| 7 | 2KI + H2O2 → I2 + 2KOH | https://topbee.vn/blog/2ki-h2o2-i2-2koh |
| 8 | 2KI + O3 + H2O → 2KOH + I2 + O2 | https://topbee.vn/blog/2ki-o3-h2o-2koh-i2-o2 |
Cân bằng PTHH KOH với chất khác





